
【题目】A~G是几种烃的分子球棍模型,据此回答下列问题:

(1)常温下含碳量最高的气态烃是________(填对应字母)。
(2)能够发生加成反应的烃有________(填数字)种。
(3)一卤代物种类最多的是________(填对应字母)。
(4)写出C与溴水反应的化学方程式:______________________。
(5)写出F发生溴代反应的化学方程式:____________________。
科目:高中化学 来源: 题型:
【题目】为探究苯与溴的取代反应,甲用如图装置Ⅰ进行如下实验:
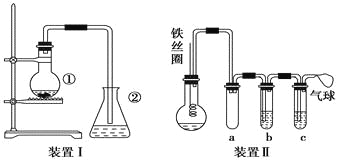
将一定量的苯和溴放在烧瓶中,同时加入少量铁屑,3~5 min后发现滴有AgNO3的锥形瓶中有浅黄色的沉淀生成,即证明苯与溴发生了取代反应。
(1)装置Ⅰ中①中的化学方程式为______________________________________。
②中离子方程式为_______________________________________。
(2)①中长导管的作用是__________________________。
(3)烧瓶中褐色油状液滴中有机物的成分是________,要想得到纯净的该产物,可用______ __洗涤。洗涤后分离粗产品应使用的仪器是____ ____。
(4)乙同学设计如图所示装置Ⅱ,并用下列某些试剂完成该实验。可选用的试剂是:苯;液溴;浓硫酸;氢氧化钠溶液;硝酸银溶液;四氯化碳。
a的作用是_______________________________________。
b中的试剂是____________________________________。
比较两套装置,装置Ⅱ的主要优点是
_____________________________________________________________
_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修3:物质结构与性质】碳、氮在自然界中广泛存在。
(1)CH3COOH中C原子轨道杂化类型有;1molCH3COOH分子中含有![]() 键的数目为
键的数目为
(2)50号元素Sn在周期表中位置是 ;写出50号元素Sn的基态原子核外电子排布式
(3)锡和碳一样能生成四氯化物(SnC14),然而锡又不同于碳,配位数可超过4.SnC14两种可能立体结构分别是 和
(4)与H20互为等电子体的一种含有碳元素的阳离子为 (填化学式);H20
与CH3CH20H可以任意比例互溶,除因为它们都是极性分子外,还因为
(5)元素X的某价态离子X}+中所有电子正好充满K, L, M三个电子层,它与
N3一形成的晶体结构如图所示。

①该晶体的阳离子与阴离子个数比为
②该晶体中Xn十离子中n=
③晶体中每个N3一被 个等距离的Xn+离子包围。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四苯基乙烯(TPE)及其衍生物具有诱导发光特性,在光电材料等领域应用前景广泛。以下是TPE的两条合成路线(部分试剂及反应条件省略):

(1)A的名称是 ;试剂Y为 。
(2)B→C的反应类型为 ;B中官能团的名称是 ,
D中官能团的名称是 。
(3)E→F的化学方程式是 。
(4)W是D的同分异构体,具有下列结构特征:①属于萘(![]() )的一元取代物;
)的一元取代物;
②存在羟甲基(-CH2OH)。写出W所有可能的结构简式: 。
(5)下列叙述正确的是______。
a. B的酸性比苯酚强
b. D不能发生还原反应
c. E含有3种不同化学环境的氢
d. TPE既属于芳香烃也属于烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用乳酸钙和FeCl2为原料生产乳酸亚铁([CH3CH(OH) COO]2Fe·3H2O) 和医用二水合氯化钙晶体(CaCl2·2H2O的质量分数为97.3% ~99.3%),制备流程如下:

(1)实验室常用两种方案制备FeCl2,写出原子利用率为100%的反应的化学方程式 ;在FeCl2溶液中需要加
(2)制备乳酸亚铁晶体是向乳酸钙溶液中加入过量的FeCl2溶液,写出该反应的化学方程式 。
(3)操作1、操作2、操作3依次为 、 、 。
(4)向“滤液a”中先加H2O2溶,作用是 。然后再调节溶液
的 pH 约为5,目的是 。
(5)向“滤液b”加盐酸的目的是 。
(6)为测定样品中CaCl2·2H2O的含量,称取0.7600g样品并配成250mL 溶液,各取该溶液 25.00mL,分别置于三个锥形瓶中,用0.05000mol·L -1 AgNO3溶液进行三次滴定,消耗AgNO3溶液的平均体积为20.39mL。计算样品中CaCl2·2H2O的质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为苯和溴的取代反应的改进实验装置图。其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入铁屑粉少量。

填写下列空白:(注:溴苯与NaOH溶液不可以发生水解反应)
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中所发生反应的化学方程式(有机物写结构简式):________________
(2)试管C中苯的作用是_________;反应开始后,观察D和E试管,看到的现象为:
D中:_______________ ;E中:___________________________ _。
(3)反应2 min至3 min后,在B中的NaOH溶液可观察到的现象是:___________________________。
(4)在上述整套装置中,具有防倒吸的仪器有________(填字母)。
(5)改进后的实验除①步骤简单,操作方便,成功率高;②各步现象明显;③对产品便于观察这3个优点外,还有一个优点是:____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应①X(g)+2Y(g)![]() 2Z(g)②2M(g)
2Z(g)②2M(g)![]() N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密闭隔板。反应开始和达到平衡状态时有关物理量的变化如图所示(隔板两侧反应室温度相同)。下列判断正确的是:
N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密闭隔板。反应开始和达到平衡状态时有关物理量的变化如图所示(隔板两侧反应室温度相同)。下列判断正确的是:

A.反应①的正反应是吸热反应
B.达平衡(I)时体系的压强与反应开始时体系的压强之比为14:15
C.达平衡(I)时X的转化率为5/11
D.在平衡(I)和平衡(II)中M的体积分数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁是重要的亚铁盐,在农业上用作农药,主要治小麦黑穗病,还可以用作除草剂;在工业上用于染色、制造蓝黑墨水和木材防腐等。
(1)新制的绿矾(FeSO4·7H2O)是浅绿色的,但在空气中极易变成黄色或铁锈色的碱式硫酸铁[Fe(OH)SO4],写出该反应的化学方程式: 。
(2)已知FeSO4在不同条件下分解得到产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2;SO3熔点是16.8℃,沸点是44.8℃。
某研究性学习小组拟用下列装置进行实验探究“在加热条件下FeSO4的分解产物”。

上述装置Ⅲ和Ⅳ用来检验气体产物。试回答下列问题:
①Ⅱ装置烧杯中水的温度应控制在 (选填“0℃、25℃、50℃”),装置Ⅱ的作用是 。
②装置Ⅲ中的试剂可以是 (选填序号,下同),现象是 ,则证明气体产物中含有SO3;装置Ⅳ中的试剂可以是 。
A.2mol/LNa2CO3溶液
B.品红溶液
C.0.5mol/L BaCl2溶液
D.0.5mol/LBa(NO3)2
E.0.01mol/L KMnO4溶液
F.淀粉碘化钾溶液
③装置V中试剂为NaOH溶液,发生反应的离子方程式为 。
④为了检验固体产物成分,取反应后的固体于试管中,加稀硫酸溶解,将所得溶液分成两份,进行如下实验:
操作步骤 | 预期实验现象 | 预期实验结论 |
向其中一份溶液中加入 | 固体中含有Fe2O3 | |
向另一份溶液中滴加2滴黄色K3[Fe(CN)6]溶液 | 产生蓝色沉淀 |
⑤若用22.8g FeSO4固体做实验,完全分解后,得到11.2g固体,其中Fe2O3的质量分数= (精确到0.1%)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸。依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体)。已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全。有关物质的沸点见下表:
![]()

请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为 (注明反应条件)。
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在_____________,目的是 ;当试管A内的主要反应完成后温度计水银球的位置应在___________________,目的是____________________。
(3)烧杯B的作用是___________________________,烧杯B内盛装的液体可以是____________(写出一种即可,在题给物质中找)。
(4)若想检验试管C中是否含有产物乙酸,请你在所提供的药品中进行选择,设计一个简便的实验方案。所提供的药品有:pH试纸、红色的石蕊试纸、白色的醋酸铅试纸、碳酸氢钠粉末。实验仪器任选。该方案为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com