
| A. | 氧化铁的化学式:FeO | |
| B. | 聚乙烯的结构简式为CH2=CH2 | |
| C. | 16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体 | |
| D. | 质子数为53,中子数为78的碘原子表示为:${\;}_{53}^{131}$I |
分析 A、氧化铁中铁为+3价,氧为-2价;
B、乙烯加聚产物为聚乙烯;
C、同种元素的不同种原子间互为同位素;同种元素形成的不同种单质间互为同素异形体;
D、质量数=质子数+中子数.
解答 解:A、氧化铁中铁为+3价,氧为-2价,故氧化铁的化学式为Fe2O3,故A错误;
B、乙烯加聚产物为聚乙烯,故聚乙烯中无碳碳双键,CH2=CH2为乙烯的结构简式,故B错误;
C、同种元素的不同种原子间互为同位素,故16O与18O互为同位素;同种元素形成的不同种单质间互为同素异形体,而H216O、D216O、H218O、D218O均为化合物,故不是同素异形体,故C错误;
D、质量数=质子数+中子数,故质子数为53,中子数为78的碘原子的质量数为131,故表示为13153I,故D正确.
故选D.
点评 本题考查了“四同”概念的辨析和常见化合物的化学式的书写以及原子的表示方法,应注意乙烯和聚乙烯的不同.


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)═2H2O(g);△H1 2H2(g)+O2(g)═2H2O(l);△H2 | |
| B. | S(s)+O2(g)═SO2(g);△H1 S(g)+O2(g)═2SO2(g);△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)═CO(g);△H1 C(s)+O2(g)═CO2(g);△H2 | |
| D. | H2(g)+Cl2(g)═2HCl(g);△H1 $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g);△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

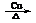 2CH3CHO+2H2O
2CH3CHO+2H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuSO4═Cu+2+SO4-2 | B. | NH4NO3═NH4++NO3- | ||
| C. | Na2CO3═Na2++CO32- | D. | KClO3═K++Cl-+3O2- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在由水电离出的c(OH-)=10-13mol/L的溶液中:Na+、Ba2+、Cl-、I- | |
| B. | 在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42-、NO3- | |
| C. | 在能使pH试纸变深蓝色的溶液中:Na+、S2-、NO3-、CO32- | |
| D. | 在pH为7的溶液中:Ag+、K+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
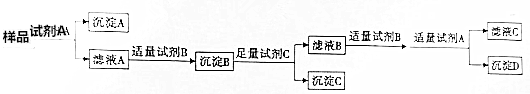
查看答案和解析>>
科目:高中化学 来源: 题型:解答题



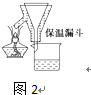
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com