
【题目】可逆反应mA(固)+nB(气)cC(气)+fD(气)反应过程中,当其它条件不变时,C的体积分数(C%)与温度(T)和压强(P)的关系如下图所示,下列叙述正确的是( ) 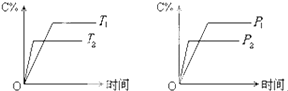
A.达到平衡后,若使用催化剂,C的体积分数增大
B.达到平衡后,若使温度升高,化学平衡向逆反应方向移动
C.化学方程式中n>c+f
D.达到化学平衡后,增加A的量有利于化学平衡向正反应方向移动
【答案】B
【解析】解:可逆反应,当其他条件一定时,温度越高,反应速率越大,达到平衡所用的时间越短.由图象(1)可知T2>T1 , 温度越高,平衡时C的体积分数φ(C)越小,故此反应的正反应为放热反应;当其他条件一定时,压强越高,反应速率越大,达到平衡所用的时间越短.由图(2)可知p2>p1 , 压强越大,平衡时C的体积分数φ(C)越小,可知正反应为气体物质的量增大的反应,即n<c+f,A、催化剂只改变化学反应速率,对平衡移动没有影响,C的体积分数不变,故A错误;
B、正反应为放热反应,升高温度平衡向吸热方向移动,即向逆反应移动,故B正确;
C、由上述分析可知,可逆反应mA(固)+nB(气)cC(气)+fD(气)正反应为气体物质的量增大的反应,即n<c+f,故C错误;
D、达平衡后,增加A的量,因为A为固体,所以平衡不移动,故D错误;
故选B.
【考点精析】利用化学平衡状态本质及特征对题目进行判断即可得到答案,需要熟知化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).


科目:高中化学 来源: 题型:
【题目】某酸性废液中含有Fe2+、Cu2+、Ba2+三种金属离子,有同学设计了下列方案对废液进行处理(所加试剂均稍过量),以回收金属,保护环境。
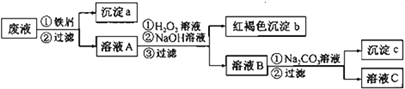
请回答:
(1)沉淀a中含有的单质是_____________。
(2)沉淀c的化学式是___________________。
(3)溶液A与H2O2溶液在酸性条件下反应的离子方程式是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自来水厂常使用氯气消毒,市场上有些小商小贩用自来水充当纯净水出售。下列试剂中,可用来辨其真伪的是( )
A. 酚酞溶液B. 氯化钡溶液C. 氢氧化钠溶液D. 硝酸银溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个密闭容器中,盛有N2和H2 , 它们的起始浓度分别是1.8molL﹣1和5.4molL﹣1 , 在一定的条件下它们反应生成NH3 , 10min后测得N2的浓度是0.8molL﹣1 , 则在这10min内NH3的平均反应速率是( )
A.0.1molL﹣1min﹣1
B.0.3molL﹣1min﹣1
C.0.2molL﹣1min﹣1
D.0.6molL﹣1min﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应2A(g)+B(g)2C(g)在反应过程中C的质量分WC随温度变化如图所示,试确定: 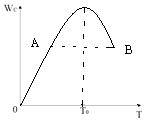
(1)T0对应的V正与V逆关系是V正V逆(填“>”、“<”、“=”).
(2)A、B两点正反应速率的大小关系VAVB(填“>”、“<”、“=”).
(3)温度T<T0时,Wc逐渐增大的原因是
(4)500℃条件下,该反应 K=2.33,测得某时刻,A(g)、B(g)、C(g)的浓度均为0.5mol/L,则此时v(正)v(逆)(填“>”“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂实验室用CO和H2制备CH3OH,其原理为:CO(g)+2H2(g)CH3OH(g)△H<0该温度下的化学平衡常数表达式;若在298K、398K时化学平衡常数分别为K1、K2 , 则K1K2(填“>”、“<”、“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的名称不正确的是
A.生石膏:CaSO4·2H2OB.摩尔盐: (NH4)2Fe (SO4)2
C.普通玻璃的成分:Na2O·CaO·6SiO2D.木精:CH3OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠、铝和铁是三种重要的金属.请回答:
Ⅰ、(1)钠原子的结构示意图是_____;铝原子的结构示意图是______.
(2)将一小块金属钠长期露置于空气中发生一系列变化,最终产物是______.
(3)取一小块金属钠放在滴有酚酞的水中,实验现象正确的是(填选项)_____.
①钠浮在水面迅速反应 ②钠沉在水底迅速反应 ③钠熔成小球并快速游动 ④反应中可以听到嘶嘶的响声 ⑤反应后的溶液变为红色
Ⅱ、(1)写出这三种金属中能与氢氧化钠溶液反应的离子方程式___________________
(2)铁、铝是常用的金属材料,在空气中铝比铁更耐腐蚀.对此合理的解释是______.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com