
 ������ʵ��д�����з�Ӧ���Ȼ�ѧ����ʽ
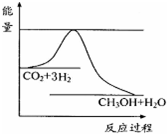
������ʵ��д�����з�Ӧ���Ȼ�ѧ����ʽ���� ��1������ͼ��֪���÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ����ʹc��CH3OH������˵��ƽ��������Ӧ�����ƶ���
��2��ȼ������1mol��ȼ����ȫȼ�������ȶ�������ʱ�ų�����������25�桢101kPa�£�1g�״���CH3OH��ȼ������CO2��Һ̬ˮʱ����22.68kJ��32g�״�ȼ������CO2��Һ̬ˮʱ����22.68kJ��32=725.76kJ��1mol�״�����Ϊ32�ˣ�������ȫȼ��1mol�״����ɶ�����̼��Һ̬ˮ����725.76KJ������ȼ���ȵĸ���������ɽ��
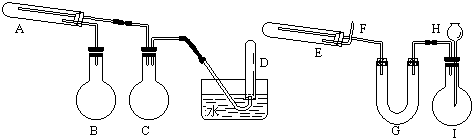
��3�����β��������������Һ�ķ��������½��裬ʹ��Һ��Ͼ��ȣ����ݽ����ĵ����Ժܺã��ᵼ��������ɢʧ����������кͷ�Ӧ���������Ȼ�ѧ����ʽ����дԭ��õ���
��4����֪��N2��g��+2O2��g���TN2O4��g������H=+8.7kJ/mol��
��N2H4��g��+O2��g���TN2��g��+2H2O��g������H=-534.7kJ/mol��
���ø�˹���ɽ��ڡ�2-�ٿɵ�2N2H4��g��+N2O4��g���T3N2��g��+4H2O��g�������Դ˼��㷴Ӧ�ȣ�
��� �⣺��1��a�������¶ȣ�ƽ�������ƶ���c��CH3OH����С����a����
b������He��g����ʹ��ϵѹǿ������������Ϊ���������������Ũ�Ȳ��䣬ƽ�ⲻ�ƶ���c��CH3OH�����䣬��b����
c����H2O��g������ϵ�з��������ƽ�������ƶ���c��CH3OH������c��ȷ��
d���ٳ���1mol CO2��3molH2��ƽ�������ƶ���c��CH3OH������d��ȷ��
�ʴ�Ϊ��cd��
��2��1mol�״���ȫȼ�����ɶ�����̼��Һ̬ˮ����725.8KJ��ȼ�����Ȼ�ѧ����ʽΪ��CH3OH��l��+$\frac{3}{2}$O2��g���TCO2��g��+2H2O��l����H=-725.8 kJ•mol-1��
�ʴ�Ϊ��CH3OH��l��+$\frac{3}{2}$O2��g���TCO2��g��+2H2O��l����H=-725.8 kJ•mol-1��
��3�����к��Ȳⶨʵ���У����β��������������Һ�ķ��������³鶯��ʹ��Һ��Ͼ��ȣ��û���ͭ˿��������滷�β���������������ĵ����Ժܺã��ᵼ��������ɢʧ��ʹ��õġ�H��ֵƫС��ϡ�����NaOHϡ��Һ��Ӧ����1molˮ����57.3KJ���÷�Ӧ���Ȼ�ѧ����ʽΪ��$\frac{1}{2}$H2SO4��aq��+NaOH��aq��=$\frac{1}{2}$Na2SO4��aq��+H2O��l����H=-57.3 kJ/mol��
�ʴ�Ϊ�����³鶯�������ĵ����Ժܺã��ᵼ��������ɢʧ��$\frac{1}{2}$H2SO4��aq��+NaOH��aq��=$\frac{1}{2}$Na2SO4��aq��+H2O��l����H=-57.3 kJ/mol��
��4����N2��g��+2O2��g��=N2O4 ��1����H1=-19.5kJ•mol-1
��N2H4 ��1��+O2��g��=N2��g��+2H2O��g����H2=-534.2kJ•mol-1
���ݸ�˹���ɼ���ڡ�2-�ٵõ��º�N2O4 ��Ӧ���Ȼ�ѧ����ʽ2N2H4 ��1��+N2O4��1���T3N2��g��+4H2O��g����H=-1048.9 kJ/mol��
�ʴ�Ϊ��2N2H4 ��1��+N2O4��1���T3N2��g��+4H2O��g����H=-1048.9 kJ/mol��
���� ������Ҫ�����˻�ѧƽ��Ӱ�����ء��Ȼ�ѧ����ʽ����д����㡢�к���ʵ������Լ��к��ȵĸ���ѶȲ���ע��ʵ��ԭ�������գ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH=12����Һ�У�K+��Na+��AlO2-��CO32- | |
| B�� | ��0.1mol•L-1��NaHCO3 ��Һ�У�K+��Al3+��I-��Cl- | |
| C�� | ��Al��Ӧ�ܷų�H2����Һ�У�Fe2+��K+��NO3-��SO42- | |
| D�� | ʹ��̪���ɫ����Һ�У�Na+��Al3+��SO42-��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͨ������ĵ缫��X��Ϊ��صĸ�����ͨ�������ĵ缫��Y��Ϊ������� | |
| B�� | �ŵ�һ��ʱ��������Һ��KOH�����ʵ������ı� | |
| C�� | �ڱ�״���£�ͨ��5.6L��������ȫ��Ӧ����1.0mol�ĵ��ӷ���ת�� | |
| D�� | �ŵ�ʱ��ͨ�������һ��������pH���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ�е�������NH3•H2O | |
| B�� | NH3�м��ԣ�������ʹʪ��ĺ�ɫʯ����ֽ����ɫ | |
| C�� | ���е���ζ�������ˮ���������ֽ� | |
| D�� | �����£�Ũ���ᡢŨ������������������Ӧ�����Կ������Ƶ���������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �٢� | C�� | �ڢ� | D�� | �ۢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com