
用NaOH固体配制1. 0 mol/L的NaOH溶液220 mL,下列说法正确的是
0 mol/L的NaOH溶液220 mL,下列说法正确的是
( )
A.首先称取NaOH固体10g
B.定容时仰视刻度线会使所配制的溶液浓度偏高
C.定容后将溶液振荡均匀,静置时发现液面低于刻度线,于是又加少量水至刻度线
D.容量瓶中原有少量蒸馏水对结果没有影响
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
某含有少量 FeCl2杂质的 FeCl3样品,现要测定其中铁元素的含量.实验步骤如下:
① 准确称量mg 样品;
② 向样品中加人 10 mL 5 mol · L一1的盐酸,再加人蒸馏水,配制成 250 mL 溶液; ③ 量取 25 mL 操作 ② 中配得的溶液,加人 3 mL 溴水,加热使之完全反应;
④ 趁热迅速加人质量分数为 10 %的氨水至过量,充分搅拌,使之完全沉淀;
⑤ 过滤,将沉淀洗涤后反复灼烧、冷却、称量至恒重。
请根据上面的叙述回答:
(1)溶解样品时要加人盐酸,其目的是_______________________________________
(2)配制 250 mL 溶液时,除需玻璃棒、烧杯外,还须用到的玻璃仪器是__________
________________________________________________
(3)加人溴水时发生反应的离子方程式是:
____________________________________________________
(4)若坩埚质量为 W1 g ,增锅与灼烧后固体的总质量是 W2 g ,则样品中铁元素的质量分数是_____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
某烃的分子式为C10H14,它不能使溴水褪色,但可使酸性KMnO4溶液褪色,分子结构中只含有一个烷基,符合条件的烃有( )
A.2种 B.3种
C.4种 D.5种
查看答案和解析>>
科目:高中化学 来源: 题型:
下列混合物中可用分液漏斗分离,且有机物应从分液漏斗的上口倒出的是( )
A.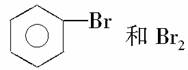
B.CH3CH2CH2CH2Cl和H2O
C.CCl4和CHCl3
D.CH2Br—CH2Br和NaBr(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
某液态卤代烃RX(R是烷基,X是某种卤素原子)的密度是a g/cm3。该RX可以跟稀碱发生水解反应生成ROH(能跟水互溶)和HX。为了测定RX的相对分子质量,拟定的实验步骤如下:
①准确量取该卤代烃b mL,放入锥形瓶中。
②在锥形瓶中加入过量稀NaOH溶液,塞上带有玻璃管的塞子,加热,发生反应。
③反应完成后,冷却溶液,加稀HNO3酸化,滴加过量AgNO3溶液得到白色沉淀。
④过滤、洗涤,干燥后称重,得到固体c g。
回答下面问题:
(1)装置中玻璃管的作用是________。
(2)步骤④中,洗涤的目的是为了除去沉淀上吸附的________离子。
(3)该卤代烃中所含卤素的名称是_______,判断的依据是______。
(4)该卤代烃的相对分子质量是________(列出算式)。
(5)如果在步骤③中,所加HNO3的量不足,没有将溶液酸化,则步骤④中测得的c值________(填下列选项代码)。
A.偏大 B.偏小
C.不变 D.大小不定
查看答案和解析>>
科目:高中化学 来源: 题型:
把500 mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为( )
A.0.1(b-2a) mol/L B.10(2a-b) mol/L
C.10(b-a) mol/L  D.10(b-2a) mol/L
D.10(b-2a) mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中物质的量浓度肯定为1 mol/L的是( )
A.将40 g NaOH固体溶解于1 L水中
B.将22.4 L氯化氢气体溶于水配成1 L溶液
C.将1 L 10 mol/L浓盐酸稀释配成10L溶液
D.10 g NaOH固体溶解在水中配成250 mL溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等。回答下列问题:
(1)铅是碳的同族元素,比碳多4个电子层。铅在元素周期表的位置为第________周期、第________族;PbO2的酸性比CO2的酸性________(填“强”或“弱”)。
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为_______________________。
(3)PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为___________________;PbO2也可以通过石墨为电极,Pb(NO3)2和Cu(NO3)2的混合溶液为电解液电解制取。阳极发生的电极反应式为____________________,阴极上观察到的现象是____________________;若电解液中不加入Cu(NO3)2,阴极发生的电极反应式为______________________________,这样做的主要缺点是____________________。
(4)PbO2在加热过程发生分解的失重曲线如下图所示,已知失重曲线上的a点为样品失重4.0%(即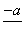 ×100%)的残留固体。若a点固体组成表示为PbOx或mPbO2·nPbO,列式计算x值和m∶n值_______________________________________
×100%)的残留固体。若a点固体组成表示为PbOx或mPbO2·nPbO,列式计算x值和m∶n值_______________________________________
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com