
|
�����£���10 mL��0.1 mol��L��1��NaOH��Һ����μ���0.1 mol��L��1������Һ�����õζ�������ͼ��ʾ������˵����ȷ����
| |
| [����] | |
A�� |
pH��7ʱ�����Ӵ�����Һ�����Ϊ10 mL |
B�� |
pH��7ʱ����Һ��c(CH3COO��)��c(Na+) |
C�� |
7��pH��13ʱ����Һ��c(Na+)��c(CH3COO��)��c(OH��)��c(H+) |
D�� |
�����μ�0.1 mol��L��1������Һ����ҺpH���Ա�Ϊ1 |
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����Ƕ�Ԫ��ǿ�ᣬ����������Һ�����ԡ������£���10 mL 0.01 mol•L-1 NaHC2O4��Һ�еμ�0.01 mol•L-1 NaOH��Һ������NaOH��Һ��������ӣ���Һ������Ũ�ȹ�ϵ��ȷ���ǣ� ��
A.V��NaOH����0ʱ��c(H+)��1��10-2mol•L-1
B.V��NaOH����10 mLʱ�������ܴ���c(Na+)��2c(C2O42-)+c(HC2O4-)
C.V��NaOH����10 mLʱ��c(H+)��1��10-7mol/L
D.V��NaOH����10 mLʱ��c(Na+)��c(C2O42-)��c(HC2O4-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013������ʡ�������и������Ĵνβ��Ի�ѧ�Ծ����������� ���ͣ���ѡ��
�����Ƕ�Ԫ��ǿ�ᣬ����������Һ�����ԡ������£���10 mL 0.01 mol/L NaHC2O4��Һ�еμ�0.01 mol/L NaOH��Һ������NaOH��Һ��������ӣ���Һ������Ũ�ȹ�ϵ��ȷ����
| A��V��NaOH����0ʱ��c(H+)��1��10-2 mol/L���� |
B��V��NaOH����10 mLʱ�������ܴ���c(Na+)��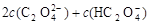 |
| C��V��NaOH����10 mLʱ��c(H+)��1��10-7 mol/L |
| D��V��NaOH����10 mLʱ��c(Na+)> c(C2O42-)> c(HC2O4-) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013����ʡ����һ�и߶���ѧ�����п��Ի�ѧ�Ծ����������� ���ͣ���ѡ��
�����Ƕ�Ԫ��ǿ�ᣬ����������Һ�����ԡ������£���10 mL 0.01 mol��L NaHC2O4��Һ�еμ�0.01 mol��L NaOH��Һ������NaOH��Һ��������ӣ���Һ������Ũ�ȹ�ϵ��ȷ����
| A��V��NaOH��="=" 0ʱ��c��H+��W��="=" 1 �� 10��2 mol��L |
B��V��NaOH��< 10 mLʱ�������ܴ���c��Na����="=" 2 c��C2O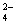 ��+ c��HC2O ��+ c��HC2O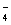 �� �� |
| C��V��NaOH��="=" 10 mLʱ��c��H+��W��="=" 1 �� 10��7mol��L |
D��V��NaOH��> 10 mLʱ��c��Na����> c��C2O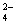 ��>c��HC2O ��>c��HC2O �� �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�꽭��ʡ�����и�����һѧ�ڼ���Ծ���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£���10 mL 0.1 mol��L-1��H2C2O4��Һ����μ���0.1 mol��L-1 KOH��Һ�����õζ�������ͼ��ʾ������˵����ȷ����

A��KHC2O4��Һ��������
B��B��ʱ��c(K+)��c(HC2O4-)��c(H+)��c(OH��)
C��C��ʱ��c(HC2O4-)+c(C2O42-)+c(H2C2O4)��c(K+)��
c(HC2O4-)+2c(C2O42-)+c(H2C2O4)
D��D��ʱ��c(H+)+ c(HC2O4-)+ c(H2C2O4)= c(OH��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ�����ʡ����һģ���ԣ����ۣ���ѧ���� ���ͣ�ѡ����
�����Ƕ�Ԫ��ǿ�ᣬ����������Һ�����ԡ������£���10 mL 0.01 mol��L NaHC2O4��Һ�еμ�0.01 mol��L NaOH��Һ������NaOH��Һ��������ӣ���Һ������Ũ�ȹ�ϵ��ȷ���ǣ�
A��V(NaOH)= 0ʱ��c(W)=1 �� 10-2 mol��L
B��V(NaOH)< 10 mLʱ�������ܴ���c(Na+)=2 c(C2O42-)+ c(HC2O4��)
C��V(NaOH)= 10 mLʱ��c(W)= 1 �� 10-7mol��L
D��V(NaOH)> 10 mLʱ��c(Na+)> c(C2O42-)>c(HC2O4-)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com