
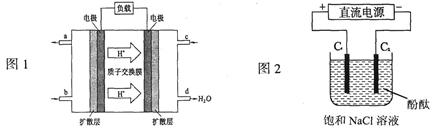
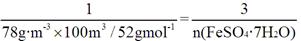

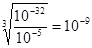 ������Һ��pH��5��
������Һ��pH��5��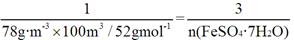



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
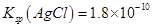 ��
�� �����й��ڲ�����֮��ת����˵���д�����ǣ�
�����й��ڲ�����֮��ת����˵���д�����ǣ�A��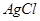 ������ˮ������ת��Ϊ ������ˮ������ת��Ϊ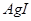 |
B�����ֲ������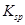 ���Խ�������Խ����ת��Ϊ�����ܵIJ����� ���Խ�������Խ����ת��Ϊ�����ܵIJ����� |
C��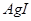 �� ��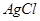 ��������ˮ�����ԣ� ��������ˮ�����ԣ�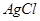 ����ת��Ϊ ����ת��Ϊ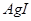 |
D�������£�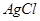 ��Ҫ�� ��Ҫ��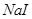 ��Һ�п�ʼת��Ϊ ��Һ�п�ʼת��Ϊ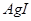 ���� ����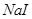 ��Ũ�ȱ��벻���� ��Ũ�ȱ��벻����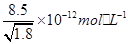 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ҹ��ϣ�AgCl��AgI�������� |
| B����AgCl��ҹ����AgNO3���壬c��Ag+������Ksp��AgCl��Ҳ���� |
| C����AgNO3����������AgCl��AgI���ɳ���������AgCl����Ϊ�� |
| D����ȡ0.235��AgI�������100ml����������仯����c��I-��=0.01mol/l |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��̼��Ʋ�����ˮ��̼��ƹ�����������ı� |
| B�����ջ�õ�̼��Ƶļ�ϡ�ı�����Һ |
| C����ΪCa2����CO32��===CaCO3������������������CaCO3===Ca2����CO32���ķ�Ӧ |
| D����Ϊ̼���������ˮ�����Ըı��������Ҳ����ı�̼��Ƶ��ܽ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ��ѧʽ | AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| �ܶȻ� | 1.4��10-10 | 1.4��10-5 | 6.3��10-50 | 7.7��10-13 | 8.51��10-16 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����Mg(OH)2����Һ�м�����NH4Cl���壬��Һ����� |
| B����AgI��ˮ�е�ƽ����ϵ�м���Na2S��Һ������ת��Ϊ��ɫ |
| C����ˮϴ��BaSO4����ϡ����ϴ����ʧ�ij���Ҫ�� |
| D��MgCO3��ˮ�м��ȿ���ת��ΪMg(OH)2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1 mol/L H2SO4��Һ | B��2 mol/L Na2SO4��Һ |
| C��0.1 mol/L BaCl2��Һ | D����ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��pHΪ12���ռ���Һ��Ba(OH)2��Һ�����ʵ���Ũ��֮�� |
| B��K2S��Һ��c(K+)��c(S2-)֮�� |
| C����ͬ�¶���0.2mol/L������Һ��0.1mol/L������Һ�е�c(H+)֮�� |
| D��10mL0.5mol/L��������5mL0.5mol/L��������Һ�е�c(H+)֮�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
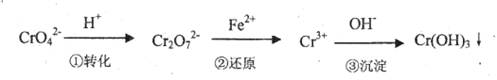
 Cr2O72-(��ɫ)+H2O
Cr2O72-(��ɫ)+H2O�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com