
分析 反应中锌从0价升高为硝酸锌中+2价,失去2个电子,硝酸中的氮从+5价,降为N2O中+1价的氮,生成1个N2O得到8个电子,依据得失电子守恒结合原子个数守恒写出反应方程式,并用双线桥表示.
解答 解:反应中锌从0价升高为硝酸锌中+2价,失去2个电子,硝酸中的氮从+5价,降为N2O中+1价的氮,生成1个N2O得到8个电子,依据氧化还原反应得失电子守恒,锌的系数为4,N2O系数为1,依据氮原子个数守恒,硝酸锌系数为4,硝酸系数为10,水系数为5,
方程式:4Zn+10HNO3=4Zn(NO3)2+N2O↑+5H2O;
依据方程式可知:反应中锌失去8mol电子,硝酸得到8mol电子,用双线桥表示为: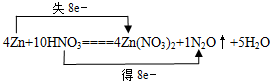 ;
;
故答案为:4;10;4;1;5; .
.
点评 本题考查了氧化还原反应方程式配平,氧化还原反应的双线桥表示,明确元素化合价变化、氧化还原反应中得失电子守恒规律是解题关键,题目难度中等.


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 酸性溶液中:Fe2+、ClO-、SO42-、Na+ | |
| B. | pH=13的无色溶液中:K+、NO3-、Al3+、CO32- | |
| C. | 澄清透明溶液中:Fe3+、Ba2+、Na+、Cl- | |
| D. | 加入铝粉后产生大量氢气的溶液中:NH4+、Na+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子数 | B. | 密度 | C. | 质量 | D. | 分子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 把Cu片和Fe片紧靠在一起浸入稀硫酸中,Cu片表面出现气泡 | |
| B. | 用铜片做阳极,铁片做阴极,电解氯化锌溶液,铁片表面出现一层铜 | |
| C. | 把Cu片浸入FeCl3溶液中,在Cu片表面出现一层铁 | |
| D. | 把Zn粒放入装有稀盐酸的试管中,加入几滴CuCl2溶液,放出气泡的速率减慢 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Na2CO3饱和溶液中,通入过量的CO2后,加热、蒸发得到NaOH晶体 | |
| B. | 向Fe2(SO4)3溶液加入足量NaOH溶液,经过过滤、洗涤沉淀,再充分灼烧沉淀得Fe2O3 | |
| C. | 向FeBr2溶液中加入过量的氯水,加热蒸发得FeCl3晶体 | |
| D. | 加热蒸发AlCl3饱和溶液得纯净的AlCl3晶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com