
��ο�����ͼ������֪E1��134 kJ��mol��1��E2��368 kJ��mol��1������Ҫ��ش����⣺
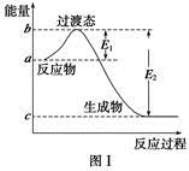
��1��ͼ����1 mol NO2(g)��1 mol CO(g)��Ӧ����CO2��NO�����е������仯ʾ��ͼ�����ڷ�Ӧ��ϵ�м����������Ӧ��������E1�ı仯�� (���������С�����䡱����ͬ)����H�ı仯�� ����д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ ��
��2���״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧ���Ȼ�ѧ����ʽ���£�
��CH3OH(g)��H2O(g)==CO2(g)��3H2(g) ��H����49.0 kJ��mol��1
��CH3OH(g)��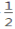 O2(g)==CO2(g)��2H2(g) ��H����192.9 kJ��mol��1
O2(g)==CO2(g)��2H2(g) ��H����192.9 kJ��mol��1
��H2O(g)==H2O(l) ��H����44 kJ��mol��1����״�����ȼ��ΪҺ̬ˮ���Ȼ�ѧ����ʽΪ ��
��3�������ʾ�Dz��ֻ�ѧ���ļ��ܲ�����
��ѧ�� | P��P | P��O | O===O | P===O |
����/kJ��mol��1 | a | b | c | x |
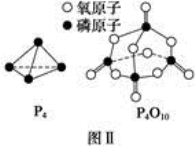
��֪����ȼ����Ϊd kJ��mol��1����������ȫȼ�յIJ���Ľṹ��ͼ����ʾ�������x�� kJ��mol��1(�ú�a��b��c��d�Ĵ�����ʽ��ʾ)��
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꼪��ʡ��һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ʵ����
ijͬѧ����ˮ�ʼ��վ����480 mL 0.5 mol��L��1NaOH��Һ�Ա�ʹ�á�
��1����ͬѧӦѡ��________mL������ƿ��ʹ������ƿǰ������е�һ��������______________
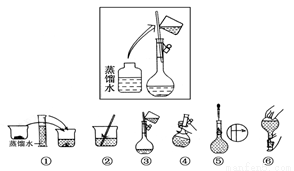
��2���������������ͼ��ʾ������ͼ����Ӧ����ͼ�е�____________����ѡ����ĸ��֮�䡣
A������� B������� C�������
��3����ͬѧӦ��ȡNaOH����________g
��4�����в�����������Һ��Ũ�ȴ�С�к�Ӱ�죿�á�ƫ�ߡ���ƫ�͡�����Ӱ�족��գ�
�ٶ���ʱ���ӿ̶��ߣ�_____________��
��ҡ�Ⱥ�Һ����ڿ̶��ߣ�û���ټ�ˮ��______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꼪��ʡ�߶���ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧһ�������Է����ǣ� ��
A��2KClO3(s)�T2KCl(s)+3O2(g)
��H=-78.03kJ��mol-1 ��S=+1110 J��mol-1��K-1
B��CO��g���TC(s��ʯī)+  O2(g)
O2(g)
��H=+110.5kJ��mol-1 ��S=-89.36 J��mol-1��K-1
C��4Fe(OH)2(s)+2H2O(l)+O2(g)�T4Fe(OH)3(s)
��H=-444.3kJ��mol-1 ��S=-280.1 J��mol-1��K-1
D��NH4HCO3(s)+CH3COOH(aq)�TCO2(g)+CH3COONH4(aq)+H2O(l)
��H=+37.301kJ��mol-1 ��S=+184.05 J��mol-1��K-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ��ɽ�и�һ��ѧ�ڽ�ѧ�ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
���������£���������������������ȵ��� �� ��
A��ͬ�¶ȡ���ͬ������N2��CO
B�����³�ѹ��ͬ�����H2O��O2
C��ͬѹǿ��ͬ���ʵ�����N2��O2
D��ͬ�¶ȡ�ͬѹǿ��ͬ�����N2O��CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ��ɽ�и�һ��ѧ�ڽ�ѧ�ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
�������Fe(OH)3���������в���ȷ���� �� ��
A���ù����ж�������� B��������ֽ
C������������ᣬ������۳� D���ܷ�����Ӿ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ��ɽ�и߶���ѧ�ڽ�ѧ�ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ΪVL���ܱ������д��ڻ�ѧƽ�⣺2NO2(g) N2O4(g)����H<0�������¶Ȳ��䣬���������ѹ����V/2������˵������ȷ���ǣ� ��
N2O4(g)����H<0�������¶Ȳ��䣬���������ѹ����V/2������˵������ȷ���ǣ� ��
A��������������ɫ���� B��������NO2����������
C����������ƽ����Է����������� D��NO2�����ʵ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ��ɽ�и߶���ѧ�ڽ�ѧ�ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
���Ȼ����ӵĿռ乹���������ζ�����ƽ���������Ρ����й������Ȼ����ӿռ乹�����ɵ���������ȷ���ǣ��� ��
A��PCl3�������������ۼ��ļ������
B��PCl3�����е�P��Cl�����ڼ��Թ��ۼ�
C��PCl3�������������ۼ��ļ��������Ǿ���ȣ�
D��PCl3������P��Cl�����������ļ�����ȣ������ڼ��Է���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ɽ��ʡ����У�߶��ϵڶ���������ѧ�Ծ��������棩 ���ͣ�ѡ����
������NH4I�����ܱ������У���һ���¶��·������з�Ӧ��
��NH4I(s) NH3(g)+HI(g)��
NH3(g)+HI(g)��
��2HI(g) H2 (g)+I2(g)��
H2 (g)+I2(g)��
��2NH3(g) N2(g)+3H2 (g)��
N2(g)+3H2 (g)��
�ﵽƽ��ʱ��c(H2) = 2 mol/L��c(N2)=0.5mol/L ��c(HI)=4mol/L����ƽ��ʱ NH3��Ũ��Ϊ
A 0.5 mol • L-1 B��2 mol • L-1 C��4 mol • L-1 D��5 mol • L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�������ʡ�����ж����ظ߶�12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
������Һ�и�����Ũ�ȹ�ϵ��˵����ȷ���ǣ� ��
A��0.1 mol•L��1 pHΪ4��NaHB��Һ�У�c(HB��)��c(H2B)��c(B2-)
B�������ʵ���Ũ�ȵ�������Һ�У���NH4Al(SO4)2����NH4Cl����CH3COONH4����NH3��H2O��c(NH4+) �ɴ�С��˳���ǣ� �٣��ڣ��ۣ���
C��a mol��L-1HCN��Һ��b mol��L-1NaOH��Һ�������Ϻ�������Һ��
c(Na��)��c(CN��)����aһ������b
D��0.1mol��L-1�Ĵ����pH��a��0.01mol��L-1�Ĵ����pH��b����a��1��b
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com