
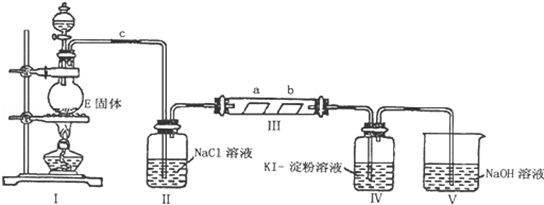

分析 装置Ⅰ中二氧化锰和浓盐酸在加热条件下反应生成氯化锰、氯气和水,生成的氯气中含氯化氢和水蒸气,通过装置Ⅱ中的饱和食盐水除去氯化氢,通过装置Ⅲ中a为干燥的品红试纸,b为湿润的品红试纸,观察颜色变化,通过装置Ⅳ中KI-淀粉溶液观察是否有蓝色出现,最后剩余氯气通入氢氧化钠溶液吸收,
(1)二氧化锰和浓盐酸在加热条件下反应生成氯化锰、氯气和水,据此写出反应的化学方程式;
(2)浓盐酸具有挥发性,所以制取的氯气中会含有氯化氢,氯气在饱和氯化钠溶液中溶解度减小,可以用饱和食盐水除去氯气中的氯化氢气体;
(3)氯气具有氧化性,能够将碘离子氧化成碘单质,据此判断装置Ⅳ中现象,然后写出反应的化学方程式;
(4)干燥的氯气不具有漂白性,Ⅱ和Ⅲ之间可加干燥装置;
(5)氯气能够与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,据此写出反应的离子方程式.
解答 解:(1)二氧化锰与浓盐酸反应制取氯气的反应的离子方程式为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
(2)装置Ⅱ中盛有饱和食盐水,由于浓盐酸具有挥发性,则制取的氯气中混有氯化氢,用饱和食盐水可以除去杂质氯化氢,
故答案为:除去氯气中的氯化氢气体;
(3)氯气具有氧化性,能够与碘化钾溶液反应生成碘单质,所以装置Ⅳ中通入氯气后,无色溶液变蓝色,反应的化学方程式为:Cl2+2KI=I2+2KCl,
故答案为:无色溶液变蓝色; Cl2+2KI=I2+2KCl;
(4)干燥的氯气不具有漂白性,Ⅱ和Ⅲ之间可加干燥装置,除去氯气中的水蒸气,
故答案为:④;干燥Cl2;
(5)装置Ⅴ盛放的是氢氧化钠溶液,目的是防止尾气污染空气,反应的化学方程式为:Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:Cl2+2OH-=Cl-+ClO-+H2O.
点评 本题考查考查物质性质实验方案的设计,题目难度中等,涉及制取气体的装置及实验方案的设计、评价等知识点,综合性较强,明确氯气的制备原理及氯气的化学性质为解答关键,试题有利于培养学生的分析、理解能力及化学实验能力.


科目:高中化学 来源: 题型:解答题

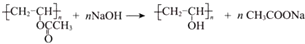 .
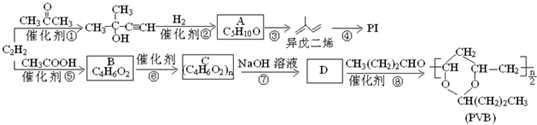
. ”改为“乙醛”,经过②、③、④后得到以顺式结构为主的高聚物,则用结构简式表示其顺式结构是
”改为“乙醛”,经过②、③、④后得到以顺式结构为主的高聚物,则用结构简式表示其顺式结构是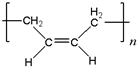 .
.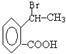 为原料合成
为原料合成 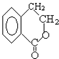 ,下列是合成流程图,在括号内注明反应条件,方框内写出有关物质的结构简式.
,下列是合成流程图,在括号内注明反应条件,方框内写出有关物质的结构简式.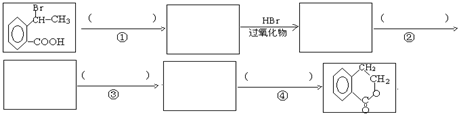
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K:1s22s22p63s23p64s1 | B. | Fˉ:1s22s22p6 | ||
| C. | Fe:1s22s22p63s23p63d54s3 | D. | Kr:1s22s22p63s23p63d104s24p6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16O2与18O2互为同位素 | |
| B. | 16O与18O核外电子排布方式不同 | |
| C. | 通过化学变化可以实现16O2与18O2间的相互转化 | |
| D. | 标准状况下,1.12L16O2和1.12L18O2均含0.1NA个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 投入铝粉产生H2的溶液中:NH4+、K+、ClO-、Cl- | |
| B. | 澄清透明的溶液中:Cu2+、SO42-、K+、NO3- | |
| C. | 有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Cl- | |
| D. | 中性的溶液中:Al3+、Na+、SO42-、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧杯中有铜、铁均有 | B. | 烧杯中Fe3+、Cu2+、Fe2+均有 | ||
| C. | 烧杯中Cu和Cu2+均有 | D. | 烧杯中Cu2+、Fe2+、Cu和Fe均有 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石蕊试纸和pH试纸使用前都必须用蒸馏水润湿 | |
| B. | 向沸水中滴加饱和氯化铁溶液并不断搅拌,制取氢氧化铁胶体 | |
| C. | 中和滴定实验时,滴定前仰视刻度,滴定后俯视,则对测得浓度无影响 | |
| D. | 滴定管盛装滴定液前需先用蒸馏水洗净,再用滴定液润洗 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com