
| A、水泥、玻璃、水晶饰物都是硅酸盐制品 |
| B、高温下,可在试管内完成焦炭和石英砂(SiO2)制取硅的反应 |
| C、透闪石的化学成分为Ca2Mg5Si8O22(OH)2写成氧化物的形式为:2CaO?5MgO?8SiO2?H2O |
| D、自然界中硅元素的贮量丰富,并存在大量的单质硅 |


科目:高中化学 来源: 题型:
| A、S(s)在O2(g)中燃烧是放热反应 |
| B、S(g)+O2(g)=SO2(g)△H=bkJ?mol-1,则a<b |
| C、1mol SO2(g)所具有的能量低于1molS(s)与1molO2(g)所具有的能量和 |
| D、16g固体硫在空气中充分燃烧,可放出-a/2kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 催化剂 |
| 1 |
| 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、用惰性电极电解氯化镁溶液:2Cl-+2H2O
| ||||
| B、一定量Cl2通入FeI2溶液中,完全反应后测得溶液中c(Fe3+)=c(Fe2+):5Cl2+8I-+2Fe2+=4I2+2Fe3++10Cl- | ||||
C、向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2Br-COOH+OH-
| ||||
| D、用氢氟酸在玻璃上“刻字”:SiO2+4H++4F-=SiF4↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使酚酞试液变红色的溶液:Na+、Ba2+、I-、Cl- |
| B、使甲基橙变红色的溶液:Ca2+、K+、HCO3-、Cl- |
| C、含有0.1mol?L-1Fe(NO3)2的溶液:H+、Mg2+、SCN-、Cl- |
| D、由水电离产生的c(H+)=10-13mol?L-1的溶液:NH4+、SO42-、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
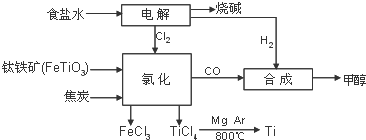 某化工厂将钛、氯碱工业和甲醇制备联合生产,大大提高原料利用率,并减少环境污染.流程如图:
某化工厂将钛、氯碱工业和甲醇制备联合生产,大大提高原料利用率,并减少环境污染.流程如图:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com