
分析 试管A的溶液中滴入酚酞试液呈粉红色,说明溶液显碱性,一定含有OH-,根据离子共存原理,一定没有Ag+、Mg2+,一定含有K+.试管B中一定含有Ag+、Mg2+,则一定没有Cl-,一定含有NO3-;
(1)根据以上分析判断试管A的溶液中存在的离子;检验钾离子用焰色反应实验;铝和碱液生成偏铝酸盐和氢气;
(2)根据试管A和B中含有的离子进行分析;
(3)分别滴加盐酸和少量Ba(OH)2,氢离子和碳酸氢根离子生成水和二氧化碳,碳酸氢根离子与氢氧化钡溶液反应生成碳酸钡沉淀和碳酸根离子,据此书写离子方程式.
解答 解:向试管A的溶液中滴入酚酞试液呈粉红色,说明溶液显碱性,一定含有OH-,根据离子共存原理,一定没有Ag+、Mg2+,一定含有K+.试管B中一定含有Ag+、Mg2+,则一定没有Cl-,一定含有NO3-;
综上所述,(1)试管A中含有K+、OH-、Cl-,试管B中含有Ag+、Mg2+、NO3-;钾离子的检验用焰色反应实验,透过蓝色钴玻璃有紫色火焰,则说明有钾离子;若向A溶液中加入铝片,铝和碱液生成偏铝酸盐和氢气,反应为:2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:K+、OH-、Cl-;焰色反应;透过蓝色钴玻璃有紫色火焰;2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)若向某试管中滴入稀盐酸产生沉淀,则该试管中含有Ag+,为试管B,
故答案为:B;
(3)若向试管A的溶液中的阳离子组成的碳酸氢盐溶液中,分别滴加盐酸和少量Ba(OH)2,则发生反应的离子方程式为:HCO3-+H+=H2O+CO2↑,Ba2++2OH-+2HCO3-=BaCO3↓+CO32-+2H2O,
故答案为:HCO3-+H+=H2O+CO2↑;Ba2++2HCO3-+2OH-=BaCO3↓+CO32-+2H2O.
点评 本题考查了离子共存及离子方程式的书写,题目难度中等,试题涉及的内容较多,充分考查了学生对所学知识的掌握情况;注意掌握离子反应发生的条件及离子方程式的书写方法.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:多选题
| A. | 蔗糖和麦芽糖的化学式都可用C12H22O11表示,它们互为同分异构体 | |
| B. | 聚乙烯、聚氯乙烯,纤维素都属于合成高分子 | |
| C. | 分馏、干馏,裂化都是化学变化 | |
| D. | 石蜡油分解产物可使溴水和酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
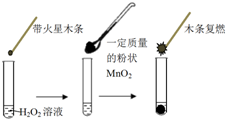 研究催化剂对化学反应有重要意义.为探究催化剂对双氧水分解的催化效果,某研究小组做了如下实验:
研究催化剂对化学反应有重要意义.为探究催化剂对双氧水分解的催化效果,某研究小组做了如下实验:| MnO2的质量/g | 0.1 | 0.2 | 0.4 |
| 40s末O2体积/mL | 49 | 61 | 86 |
| 试管 | Ⅰ | Ⅱ | Ⅲ |
| 滴加试剂 | 5滴0.1mol•L-1FeCl3 | 5滴0.1mol•L-1 CuCl2 | 5滴0.3mol•L-1 NaCl |
| 产生气泡情况 | 较快产生细小气泡 | 缓慢产生细小气泡 | 无气泡产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| AgCl | Ag2CrO4 | Ag2S | AgBr | AgI | |
| 颜色 | 白色 | 橘红色 | 黑色 | 淡黄色 | 黄色 |
| Ksp | 1.8×10-10 | 1.1×10-12 | 6.0×10-50 | 7.7×10-13 | 8.5×10-16 |
| A. | 往Ag2S悬浊液中加入少量K2CrO4溶液,沉淀将由黑色变成橘红色 | |
| B. | 反应2AgCl(s)+S2-(aq)?Ag2S(s)+2Cl-(aq)的平衡常数K=5.4×1029 | |
| C. | 用AgNO3标准溶液测定溶液中的c(Cl-),可用K2CrO4或K2S溶液作指示剂 | |
| D. | 在20mL浓度均为1.8×10-6mol•L-1的Cl-、Br-及I-的混合溶液中,逐滴(1滴约0.05mL)加入0.01mol•L-1的AgNO3溶液,可依次得到AgCl、AgBr和AgI沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
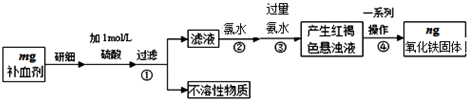
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com