
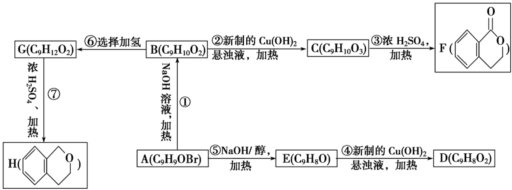
 ,B为
,B为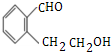 ,B选择加氢生成G,为还原反应,G在浓硫酸作用下分子内脱水,形成成醚键,是取代反应,结合G的分子式和H的结构简式可推知,G为
,B选择加氢生成G,为还原反应,G在浓硫酸作用下分子内脱水,形成成醚键,是取代反应,结合G的分子式和H的结构简式可推知,G为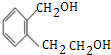 ,由A→B的关系A中氢氧化钠溶液中卤原子发生取代反应得B,可推知A为
,由A→B的关系A中氢氧化钠溶液中卤原子发生取代反应得B,可推知A为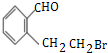 ,A在氢氧化钠醇溶液中发生消去反应生成E为
,A在氢氧化钠醇溶液中发生消去反应生成E为 ,E再被氧化生成D为
,E再被氧化生成D为 ,据此答题;
,据此答题; ,B为
,B为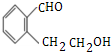 ,B选择加氢生成G,为还原反应,G在浓硫酸作用下分子内脱水,形成成醚键,是取代反应,结合G的分子式和H的结构简式可推知,G为
,B选择加氢生成G,为还原反应,G在浓硫酸作用下分子内脱水,形成成醚键,是取代反应,结合G的分子式和H的结构简式可推知,G为 ,由A→B的关系A中氢氧化钠溶液中卤原子发生取代反应得B,可推知A为
,由A→B的关系A中氢氧化钠溶液中卤原子发生取代反应得B,可推知A为 ,A在氢氧化钠醇溶液中发生消去反应生成E为
,A在氢氧化钠醇溶液中发生消去反应生成E为 ,E再被氧化生成D为
,E再被氧化生成D为 ,
,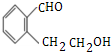 ,
,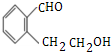 ;
; ,含有羧基和碳碳双键,F中有酯基,所以可以选择溴的四氯化碳溶液(或Na2CO3溶液)来鉴别它们,
,含有羧基和碳碳双键,F中有酯基,所以可以选择溴的四氯化碳溶液(或Na2CO3溶液)来鉴别它们,
| 浓H2SO4 |
| △ |
 +H2O,
+H2O,
| 浓H2SO4 |
| △ |
 +H2O;
+H2O; ,
, ;
;


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
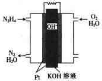 燃料电池在工业生产中有重要用途,肼(N2H4)燃料电池方产物对环境无污染,能量高,有广泛的应用前景,其工作原理如图所示.回答下列问题:
燃料电池在工业生产中有重要用途,肼(N2H4)燃料电池方产物对环境无污染,能量高,有广泛的应用前景,其工作原理如图所示.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
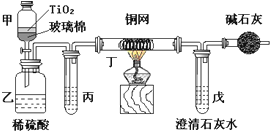 电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成OCN-,再在酸性条件下继续被NaClO氧化成N2和CO2.
电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成OCN-,再在酸性条件下继续被NaClO氧化成N2和CO2.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25% |
| B、20.75% |
| C、17.85% |
| D、26.45% |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
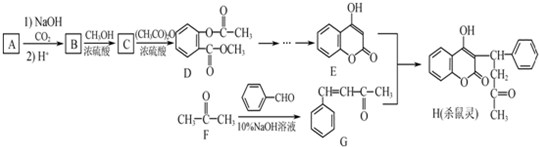
 为原料制备
为原料制备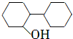 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:| NaOH醇溶液 |
| △ |
| H2 |
| Ni/△ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com