
(满分12分)用中和滴定法测定某烧碱样品的纯度。
⑴ 配制待测液: 将0.85g含有少量杂质(不与盐酸反应)的固体烧碱样品配制成100mL溶液,所用的主要仪器有___________________________________________。
⑵ 滴定: ①盛装0.20mol/L盐酸标准液应该用_______滴定管。
②滴定时,应先向锥形瓶中加酚酞作为指示剂;滴定过程中两眼应该注视________,滴定终点时,锥形瓶中的溶液的颜色变化是__________。
③有关数据记录如下:
|
滴定序号 |
待测液体积 (mL) |
所消耗盐酸标准液的体积(mL) |
|
|
滴定前 |
滴定后 |
||
|
1 |
20.00 |
0.50 |
20.70 |
|
2 |
20.00 |
6.00 |
26.00 |
⑶ 纯度计算:NaOH溶液的浓度为____________mol/L,烧碱样品的纯度为_________。
⑷ 对几种假定情况的讨论(填无影响、偏高、偏低)
①若刚见到指示剂局部的颜色有变化就停止滴定,则会使测定结果_________。
②读数时,若滴定前仰视,滴定后俯视,则会使测定结果_________________。
(1)烧杯、玻璃棒、100mL容量瓶、胶头滴管(2分);
(2)①酸式 (1分), ②锥形瓶内溶液的颜色变化和滴定速度(2分);
红色刚好变成无色且30秒钟内不恢复原色(1分)。
⑶ 0.201 (2分) , 94.6%(2分) ;
⑷ ①偏低(1分), ② 偏低(1分)。
【解析】(1)考查常见的基本实验操作。准确配制一定物质的量浓度的溶液所需要的主要仪器有容量瓶、烧杯、玻璃棒和胶头滴管。
(2)滴定管分为酸式和碱式两种滴定管。盐酸应放在酸式滴定管中。在滴定过程中,眼睛必须注视锥形瓶内溶液颜色的变化。用酚酞作指示剂,盐酸滴定氢氧化钠溶液终点的颜色变化为溶液由红色变为无色,且在半分钟内不褪色。
(3)两次实验中消耗盐酸的体积分别是20.20ml和20.00ml,所以平均值为2010ml,因此氢氧化钠的浓度是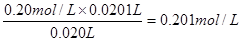 。所以样品的纯度是
。所以样品的纯度是
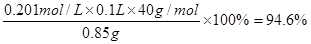 。
。
(4)若刚见到指示剂局部的颜色有变化就停止滴定,说明盐酸不足,测定结果偏低。若滴定前仰视,读数偏大,滴定后俯视,读数偏小,所以消耗的盐酸体积偏小,测定结果偏低。


科目:高中化学 来源: 题型:
(满分12分)用中和滴定法测定某烧碱样品的纯度。
⑴ 配制待测液: 将0.85g含有少量杂质(不与盐酸反应)的固体烧碱样品配制成100mL溶液,所用的主要仪器有___________________________________________。
⑵ 滴定: ①盛装0.20mol/L盐酸标准液应该用_______滴定管。
②滴定时,应先向锥形瓶中加酚酞作为指示剂;滴定过程中两眼应该注视________,滴定终点时,锥形瓶中的溶液的颜色变化是__________。
③有关数据记录如下:
| 滴定序号 | 待测液体积 (mL) | 所消耗盐酸标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.70 |
| 2 | 20.00 | 6.00 | 26.00 |
⑶ 纯度计算:NaOH溶液的浓度为____________mol/L,烧碱样品的纯度为_________。
⑷ 对几种假定情况的讨论(填无影响、偏高、偏低)
①若刚见到指示剂局部的颜色有变化就停止滴定,则会使测定结果_________。
②读数时,若滴定前仰视,滴定后俯视,则会使测定结果_________________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年广东省深圳高级中学高二下学期期中化学试卷(带解析) 题型:实验题
(满分12分)用中和滴定法测定某烧碱样品的纯度。
⑴配制待测液: 将0.85g含有少量杂质(不与盐酸反应)的固体烧碱样品配制成100mL溶液,所用的主要仪器有___________________________________________。
⑵滴定: ①盛装0.20mol/L盐酸标准液应该用_______滴定管。
②滴定时,应先向锥形瓶中加酚酞作为指示剂;滴定过程中两眼应该注视________,滴定终点时,锥形瓶中的溶液的颜色变化是__________。
③有关数据记录如下:
| 滴定序号 | 待测液体积 (mL) | 所消耗盐酸标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.70 |
| 2 | 20.00 | 6.00 | 26.00 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com