
| A. | 野火烧不尽,春风吹又生 | B. | 爆竹声中一岁除,春风送暖入屠苏 | ||
| C. | 春蚕到死丝方尽,蜡炬成灰泪始干 | D. | 粉身碎骨浑不怕,要留清白在人间 |
科目:高中化学 来源: 题型:选择题
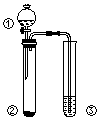 利用如图所示装置进行下列实验,能得出相应实验结论的是( )
利用如图所示装置进行下列实验,能得出相应实验结论的是( )| 选项 | ① | ② | ③ | 实验结论 |
| A | 浓盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:C>Si |
| B | 食盐水 | 电石 | 溴水 | 乙炔可与溴发生加成反应 |
| C | 浓硝酸 | Fe | NaOH溶液 | 铁和浓硝酸反应可生成NO2 |
| D | 浓硫酸 | Na2SO3 | KMnO4酸性溶液 | SO2具有还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 至少存在5种离子 | |
| B. | Cl-一定存在,且 c (Cl-)>0.4mol/L | |
| C. | SO42-、NH4+、一定存在,Cl-可能不存在 | |
| D. | CO32-、Al3+-定不存在,K+可能存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶格能指形成1mol离子键所放出的能量 | |
| B. | 晶格能指破坏1mol离子键所吸收的能量 | |
| C. | 晶格能指1mol离子化合物中的阴、阳离子由相互远离的气态离子结合成离子晶体时所放出的能量 | |
| D. | 晶格能的大小与晶体的熔点,硬度无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 集中处理废旧电池,以防止重金属污染 | |
| B. | 食用含铁丰富的食物,可预防缺铁性贫血 | |
| C. | 使用加碘食盐,可预防因缺碘引起的甲状腺肿大 | |
| D. | 大量使用食品添加剂,可使食品营养更丰富 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
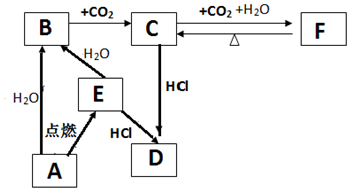
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com