
【题目】B、N、Co均为新型材料的重要组成元素,请回答下列问题:
⑴基态Co原子核外电子占据________种不同的能级,其中有________个未成对电子。
⑵Co能形成[Co(CNO)6]3-
①1 mol该离子中含有δ键的数目为________。
②与CNO-互为等电子体的分子为________(填化学式,任写一种)。
③相同压强下,CO晶体的熔点高于N2晶体的原因是________。
⑶氟硼酸铵(NH4BF4)用作铝、铜和铝合金焊接助熔剂、镁铸件防氧化添加剂、阻燃剂、农用杀虫、杀菌剂、树脂黏结剂等.是合成氮化硼纳米管的原料之一。
①1 mol NH4BF4含有_______ mol配位键。
②第一电离能大小介于B和N之间的基态原子第一电离能由大到小的顺序为________(用元素符号表示)。
③BF4-的空间立体构型为________,其中硼原子的杂化轨道类型为________。
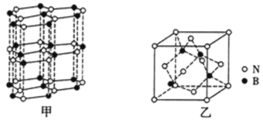
④BN晶体有多种结构,其中六方相氮化硼![]() 如图甲
如图甲![]() 是通常存在的稳定相,其结构与石墨相似却不导电,原因是_______,而立方氮化硼具有金刚石型结构,其晶胞如图乙所示,若晶胞参数为a pm,晶胞密度为d gcm-3,则阿伏加德罗常数的值可表示为________mol-1。
是通常存在的稳定相,其结构与石墨相似却不导电,原因是_______,而立方氮化硼具有金刚石型结构,其晶胞如图乙所示,若晶胞参数为a pm,晶胞密度为d gcm-3,则阿伏加德罗常数的值可表示为________mol-1。
【答案】7 3 18NA(或18×6.02×1023等合理答案即可) CO2(或CS2或N2O等) CO为极性分子,N2为非极性分子,CO分子间的范德华力更大 2 O > C > Be 正四面体 sp3杂化 层状结构中没有自由移动的电子 ![]()
【解析】
⑴基态Co原子核外电子排布式为1s22s22p63s23p63d74s2。
⑵①1 mol该离子中含有δ键的数目为3×6NA;②N = C-或O = N-来书写与CNO-互为等电子体的分子;③相同压强下,CO晶体的熔点高于N2晶体的原因是CO为极性分子,N2为非极性分子。
⑶① NH4+中N原子和其中一个H原子之间存在配位键、BF4-中B原子和其中一个F原子之间存在一个配位键;② Be中2s轨道电子处于全充满状态和N中2p轨道电子处于半充满状态,较稳定;③BF4-中中心原子B的价层电子对数为4对;④六方相氮化硼结构与石墨相似却不导电,原因是B原子的价电子全部参与成键,立方氮化硼先计算胞中N原子,B原子个数4,再根据立方氮化硼的密度。
⑴基态Co原子核外电子排布式为1s22s22p63s23p63d74s2,原子核外电子占据1s、2s、2p、3s、3p、3d、4s共7种不同的能级,其中有3个未成对电子;故答案为:7;3。
⑵①1 mol该离子中含有δ键的数目为3×6NA或18×6.02×1023;故答案为:18NA(或18×6.02×1023等合理答案即可)。
②与CNO-互为等电子体的分子为CO2或CO2或N2O等;故答案为:CO2(CO2或N2O等)。
③相同压强下,CO晶体的熔点高于N2晶体的原因是CO为极性分子,N2为非极性分子,CO分子间的范德华力更大;故答案为:CO为极性分子,N2为非极性分子,CO分子间的范德华力更大。
⑶①NH4BF4中, NH4+中N原子和其中一个H原子之间存在配位键、BF4-中B原子和其中一个F原子之间存在一个配位键,所以含有2个配位键,则1 mol NH4BF4含有2mol配位键;故答案为:2。
②同一周期从左到右第一电离能逐渐增大,因Be中2s轨道电子处于全充满状态和N中2p轨道电子处于半充满状态,较稳定,第一电离能变大,故第一电离能处在B和N之间的有Be、C、O,三种基态原子的第一电离能由大到小的顺序为O > C > Be;故答案为:O > C > Be。
③BF4-中中心原子B的价层电子对数为4对,故空间立体构型为正四面体,其中B原子的杂化形式为sp3杂化;故答案为:正四面体;sp3杂化。
④六方相氮化硼结构与石墨相似却不导电,原因是B原子的价电子全部参与成键,故其层状结构中没有自由移动的电子;立方氮化硼中,晶胞中N原子个数![]() ,B原子个数也为4,立方氮化硼的密度
,B原子个数也为4,立方氮化硼的密度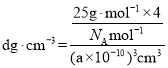 ,
,![]() ;故答案为:层状结构中没有自由移动的电子;
;故答案为:层状结构中没有自由移动的电子;![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列化学实验事实及其解释都正确的是( )
A.将饱和氯水滴到淀粉碘化钾试纸上出现如图所示的现象,说明低浓度氯水能将I-氧化成I2,高浓度氯水能将I2进一步氧化成碘的化合物
B.将过量CO2通入Ca(ClO)2溶液中得到澄清溶液,说明H2CO3的酸性比HClO的弱
C.用饱和Na2CO3溶液可将BaSO4转化为BaCO3,说明Ksp(BaSO4)>Ksp(BaCO3)
D.铝箔在酒精灯火焰上加热熔化,但不滴落,说明铝箔表面的氧化铝膜的熔点低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 时,三种酸的电离平衡常数如下:
时,三种酸的电离平衡常数如下:
化学式 |
|
| HClO |
电离平衡常数 |
|
|
|
回答下列问题:
(1)一般情况下,当温度升高时,![]() ______填“增大”、“减小”或“不变”。
______填“增大”、“减小”或“不变”。
(2)下列四种离子结合质子能力由大到小的顺序是______填序号;
a、CO32- b、ClO- c、CH3COO- d、HCO3-
(3)下列反应不能发生的是______填序号
a. ![]()
b. ![]()
c. ![]()
d. ![]()
(4)用蒸馏水稀释![]() 的醋酸,下列各式表示的数值随水量的增加而增大的是______填序号;
的醋酸,下列各式表示的数值随水量的增加而增大的是______填序号;
a. 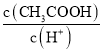 b.
b. ![]() c.
c.![]() d.
d.![]()
(5)体积均为10mLpH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。
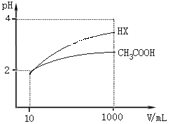
则HX的电离平衡常数______填“大于”、“等于”或“小于”,下同醋酸的电离平衡常数;稀释后,HX溶液中水电离出来的c(H+)______醋酸溶液中水电离出来的c(H+),理由是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列各组离子在指定溶液中一定能大量共存的是
A.0.1mol·L-1 AlC13溶液中:H+、Na+、Cl-、SO![]()
B.含有0.1mol·L-1 Fe3+的溶液中:Na+、K+、SCN-、NO![]()
C.使甲基橙变红色的溶液中:Fe2+、K+、NO![]() 、SO
、SO![]()
D.由水电离产生的c(H+)=10-12 mol·L-1的溶液中:NH![]() 、SO
、SO![]() 、HCO
、HCO![]() 、Cl-
、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤和石油是化工原料的重要来源,从石油中获得A,是工业上生产A的主要途径,A可用作植物生长调节剂。从煤焦油中可获得烃B,B中碳、氢两种元素的质量比为12:1,且B是常见的有机溶剂。工业上可以通过以下途径获得A、B。
![]()
![]()
(1)由煤得到煤焦油的方法称为________;由石蜡油获得A的方法称为________。
(2)A和B中,能使酸性高锰酸钾溶液褪色的是________(填“A”或“B”)。
(3)写出B发生取代反应的化学方程式:________________________(写一个即可,并注明反应条件)。
(4)用B和丙烯可以生产两种重要的化工原料:苯酚(![]() )和丙酮(
)和丙酮(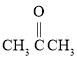 ),生产流程如下:
),生产流程如下:
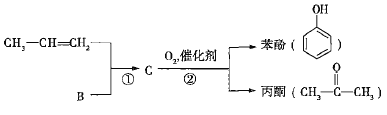
已知反应①是加成反应,C的一氯代物有5种,则C的结构简式为_____________;反应②的化学方程式为_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在![]() 时,某溶液中,
时,某溶液中,![]() 、
、![]() 、
、![]() 三者所占的物质的量分数
三者所占的物质的量分数![]() 随溶液pH变化关系如下图所示,下列叙述错误的是
随溶液pH变化关系如下图所示,下列叙述错误的是

A.![]() 是二元弱酸,其
是二元弱酸,其![]()
B.![]() 时,
时,![]() ,溶液中还存在
,溶液中还存在![]() 分子
分子
C.NaHR在溶液中![]() 电离程度大于水解程度
电离程度大于水解程度
D.将相同物质的量![]() 与NaHR固体完全溶于水可配得pH为
与NaHR固体完全溶于水可配得pH为![]() 的混合液
的混合液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于![]() 说法正确的是( )
说法正确的是( )
A.同一条直线上碳原子有6个
B.所有原子可能在同一平面上
C.同一平面上的原子最多有19个
D.所有碳原子不可能在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,现有![]() 的
的![]() 溶液,
溶液,![]() 已知含氮
已知含氮![]() 或含碳
或含碳![]() 各微粒的分布分数
各微粒的分布分数![]() 平衡时某种微粒的浓度占各种微粒浓度之和的分数
平衡时某种微粒的浓度占各种微粒浓度之和的分数![]() 与pH的关系如图所示。下列说法不正确的是
与pH的关系如图所示。下列说法不正确的是![]()
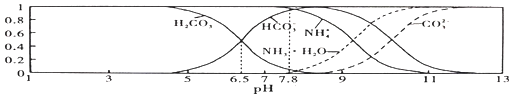
A.常温下![]()
B.向![]() 的上述溶液中逐滴滴加NaOH溶液时,
的上述溶液中逐滴滴加NaOH溶液时,![]() 和
和![]() 浓度都逐渐减小
浓度都逐渐减小
C.![]() 溶液中存在下列守恒关系:
溶液中存在下列守恒关系:![]()
D.当溶液的![]() 时,溶液中存在下列关系:
时,溶液中存在下列关系:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以淀粉和油脂为原料,制备生活中某些物质。
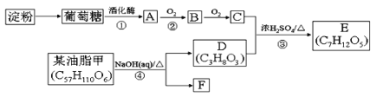
请回答下列问题:
(1)淀粉的分子式为____。
(2)③的反应类型___。
(3)写出反应①的化学方程式:____。写出反应④的化学方程式:____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com