
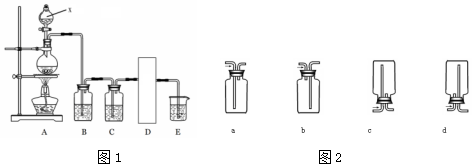
 MnCl2+Cl2↑+2H2O.
MnCl2+Cl2↑+2H2O.分析 本实验通过装置A制取氯气,涉及的原理是:MnO2+4HCl (浓) MnCl2+Cl2↑+2H2O,由于浓盐酸具有挥发性,制得的氯气不纯,装置B用饱和的食盐水,目的是除去氯化氢得到洁净的氯气,由于氯气表面沾有水分,通过装置C浓硫酸除水,接着通过装置D收集气体,最后用E进行尾气处理,因为氯气有毒.
MnCl2+Cl2↑+2H2O,由于浓盐酸具有挥发性,制得的氯气不纯,装置B用饱和的食盐水,目的是除去氯化氢得到洁净的氯气,由于氯气表面沾有水分,通过装置C浓硫酸除水,接着通过装置D收集气体,最后用E进行尾气处理,因为氯气有毒.
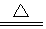
(1)x仪器名称是分液漏斗,所盛放试剂是液体浓盐酸;氯气密度比空气大,用向上排空气法收集;
(2)加热条件下,浓盐酸和二氧化锰发生氧化还原反应生成氯化锰、氯气和水;
(3)因氯气难溶于饱和食盐水,氯化氢极易溶于水,则除去Cl2中的HCl可通过饱和食盐水;
(4)氯气有毒不能直接排放到空气中,用NaOH吸收反应生成NaCl、NaClO和H2O;
解答 解:(1)装置中添加浓盐酸通过分液漏斗,所以x仪器名称是分液漏斗;氯气密度比空气大,应用向上排空气法收集,故选ad,
故答案为:分液漏斗;ad
(2)加热条件下,浓盐酸和二氧化锰反应生成氯化锰、氯气和水,反应方程式为:MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O,
MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(3)因浓盐酸具有挥发性,制得的氯气中混有HCl气体,又因氯气难溶于饱和食盐水,则可将气体通过饱和食盐水,以除去HCl,
故答案为:饱和食盐水;除去氯气中的HCl
(4)氯气有毒不能直接排放到空气中,应用NaOH吸收反应生成NaCl、NaClO和H2O,故方程式为:Cl2+2NaOH=NaCl+NaClO+H2O,
故答案为:Cl2+2NaOH=NaCl+NaClO+H2O
点评 本题考查了氯气的制备和性质的检验,熟悉反应原理及氯气的化学性质是解题关键,本题较为简单.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 铁表面镀锌可增强其抗腐蚀性 | |
| B. | 为防止月饼等富脂食品氧化变质,常在包装袋中放入生石灰 | |
| C. | “青蒿一握,以水二升渍,绞取汁”,上述对青篙素的提取过程属于物理变化 | |
| D. | 含重金属离子的电镀废液不能随意排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D、E五种元素的原子序数依次增大.A是原子半价最小的元素;B的最外层电子数是次外层电子数的2倍; D的L能层有两对成对电子;E+的核外有三个能层,且都外于全满状态.试回答下列问题:
A、B、C、D、E五种元素的原子序数依次增大.A是原子半价最小的元素;B的最外层电子数是次外层电子数的2倍; D的L能层有两对成对电子;E+的核外有三个能层,且都外于全满状态.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铯是一种强碱,比KOH的碱性强 | |
| B. | 铯与水或酸溶液反应剧烈,都生成氢气 | |
| C. | Cs的还原性比Na强,故Na+的氧化性大于Cs+ | |
| D. | Al的金属性大于Cs的金属性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应速率:前者快,后者慢 | |
| B. | 消耗硝酸的物质的量:前者多,后者少 | |
| C. | 反应生成相同条件下气体的体积:前者多,后者少 | |
| D. | 反应中转移的电子总数:前者多,后者少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| a | CO2 | Al(OH)3 | H2SO4 | HNO3 |
| b | Na2CO3 | NaAlO2 | SO2 | NO |
| c | NaHCO3 | Al2O3 | SO3 | NO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com