
����Ŀ������ͭ��һ�ֺ�ɫ���壬������ϡ���ᡣijͬѧ��֪��ϡ�����е���������(H2O��H����SO![]() )��ʹ����ͭ�ܽ⡣�������һ��ͨ����ͼ��ʾ������͢�����ʵ��������̽�����
)��ʹ����ͭ�ܽ⡣�������һ��ͨ����ͼ��ʾ������͢�����ʵ��������̽�����
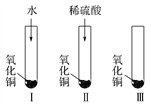
(1)ͨ��ʵ������֤��____________________________________��
(2)Ҫ֤���������������ܷ��ܽ�����ͭ������Ҫ����ʵ���͢��ڢ��м���ϡ���������ͭ�ܽ⣬���һ��ȷ�ϵ�ʵ������ǣ��ڢ����ȼ���________���ټ���________��
(3)̽�����Ϊ_____________________________________________��
(4)��Ӧ�����ӷ���ʽΪ____________________________________________________��
���𰸡� ˮ����ʹ����ͭ�ܽ� ������������ ϡ���� H�����ܽ�����ͭ����H2O��SO![]() �������Ӷ�����ʹCuO�ܽ� CuO��2H��===Cu2����H2O
�������Ӷ�����ʹCuO�ܽ� CuO��2H��===Cu2����H2O
��������(1)ʵ�����Թ��е�Һ��ɷ�Ϊˮ����ʵ��֤��ˮ���ܽ�CuO��
(2)Ҫ��֤�������õ���H+������Ҫ�ų�SO42-�ĸ��ţ������ڢ���Ӧ�ü�������������Σ���Na2SO4(��K2SO4��)������ټӷ�ϡ������
(3)ͨ���Ա�ʵ����֤�����õijɷ֣��ó������ǣ�����ͭ��������ϡH2SO4��ϡ����H+�������ã���H2O��SO42-�������Ӷ�����ʹCuO�ܽ⣻
(4)CuO���������������ӷ�Ӧ����ͭ���Ӻ�ˮ����Ӧ�����ӷ���ʽΪ��CuO+2H+=Cu2++H2O��


 Ӧ�����������Ĵ���ѧ������ϵ�д�
Ӧ�����������Ĵ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���1.5mol �����������У���ȷ���ǣ� ��
A. ������ 4g
B. ����� 33.6L
C. �������� 3
D. ������ԼΪ1.5��6.02��1023��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�0.1mol/L��H2C2O4��Һ��H2C2O4��HC2O4����C2O42����������ռ���ʵ����������ֲ�ϵ������pH�仯�Ĺ�ϵ��ͼ��ʾ�����б�������ȷ���ǣ� �� 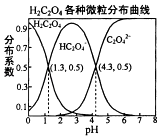
A.HC2O4��H++C2O42�� �� K=1��10��4.3
B.�������ʵ�����NaHC2O4��NAa2C2O4����ˮ�У�������ҺPHǡ��Ϊ4.3
C.������HF��KB=1��10����3.45 �� ������H2C2O4��Һ���뵽����NaF��Һ�У������ķ�ӦΪ��H2C2O4+F��=HF+HC2O4��
D.��0.1mol/LNaHC2O4��Һ�У�������Ũ�ȴ�С��ϵΪ��c��Na+����c��HC2O4������c��C2O42������c��OH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ӧ�û���ʵ�뽺�������û�й�ϵ����
A. ��������������ˮ
B. ��ʯ�����±���ƶ���
C. ��FeCl3��Һ�еμ�NaOH��Һ���ֺ��ɫ����
D. �峿�������ï�ܵ���ľ֦Ҷ���������������������Ĺ��ߣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��a mol FeS��b mol FeOͶ�뵽VL cmol/L��������Һ�г�ַ�Ӧ������NO���壬���ó�����Һ�ɷֿɿ�����Fe(NO3)3��H2SO4�Ļ��Һ����Ӧ��δ����ԭ���������Ϊ
�� (3a+3b)mol ��[Vc-(9a+b)/3]mol �� Vc-(a+b)/3 mol ��(a+b)��189g
A. �٢ڢ� B. �٢� C. �ڢ� D. �ڢۢ�
���𰸡�A
����������Ӧ���е���Ԫ��ת��ΪFe(NO3)3����Ӧ��δ����ԭ���������Ϊ��(3a+3b)mol���(a+b)��189g��amolFeS��bmolFeOת��ΪFe(NO3)3��H2SO4��ʧȥ����(9a+b)mol�����ݵ�ʧ������Ŀ��ȿ�֪����NO(9a+b)/3mol����Ӧ��δ����ԭ���������Ϊ��[Vc-(9a+b)/3]mol����֮����Ӧ��δ����ԭ���������Ϊ�٢ڢܣ���ѡA��
�����͡���ѡ��
��������
25
����Ŀ����1���ڷ�Ӧʽ:aFeCl2+bKNO3+cHCl=dFeCl3+eKCl+fX+gH2O�У���b=1��d=3����X�ķ���ʽΪ____________��
��2���������������ԭ��Ӧ�����ӷ�Ӧ����ʽ�����������ת�Ƶķ������Ŀ��___________
___CrI3+____Cl2+______����____K2CrO4+____KIO4+___KCl+______
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ѧ��ʵʩ��һ������ɫ�ƻ�����ͨ����������̼�õ�̼���ϣ�����ԭ����ͼ��ʾ���������õõ���̼������������ӵ�أ�����˵����ȷ���ǣ� �� 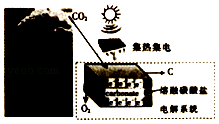
A.ͼ����������ʽֻ��һ��
B.�����ĵ缫��ӦʽΪ2CO32����4e��=2CO2��+O2��
C.����Ӧ��ת��1mole�� �� ������������CO32��0.5mol
D.������12g̼����ʱ�����ռ���22.4L O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ����Ҫ������
��1���������������ȷ�Ӧ���Ӹֹ죬������������������Ӧ�Ļ�ѧ����ʽΪ��_____________________ ��
��2����������ұ���۵�ϸߵĽ����緰�������̵ȣ�����ƽ��������ұ���������Ļ�ѧ��Ӧ����ʽ��_____ V2O5 + Al ![]() Al2O3 + V���÷�Ӧ����������__________________ ��Ҫ�õ�1mol����������Ҫ����������__________g��
Al2O3 + V���÷�Ӧ����������__________________ ��Ҫ�õ�1mol����������Ҫ����������__________g��
��3������NaOH��Һ��Ӧ�����ӷ���ʽΪ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����(����)
A. �����ʶ�����C��H��N��O����Ԫ����ɵ�
B. ��Ȼ������ˮ������ղ����Ϊ��������
C. ǿ�ᡢǿ����ؽ����ζ���ʹ�����ʱ���
D. ���ɵ����ʵ�ijЩ���������������Dz��ܺϳɵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�У�c��H+��������( )
A. 0.1 mol/L HCl��Һ B. 0.1 mol/L NaOH��Һ
C. 0.1 mol/L H2SO4��Һ D. 0.1 mol/L CH3COOH��Һ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com