

分析 实验室用NaClO3制取ClO2气体,再由ClO2制得NaClO2,由实验装置可知,A中发生2NaClO3+Na2SO3+H2SO4=2Na2SO4+2ClO2↑+H2O,必须使NaClO3稍微过量时防止生成二氧化硫,C中发生2ClO2+2NaOH+H2O2=2NaClO2+2H2O+O2,由信息高于38°C时析出晶体是NaClO2,可知温度在55°C左右,蒸发结晶、过滤、洗涤、干燥得到NaClO2,NaClO2具有氧化性时可氧化亚铁离子;B作安全瓶,D吸收尾气,NaOH溶液吸收多余的ClO2,生成物质的量之比为1:1的两种阴离子,一种为ClO2-,由Cl元素的化合价降低可知,另一种离子中Cl离子化合物为+5价,
(1)装置B中制备得到ClO2,所以B中反应为NaClO3和Na2SO3在浓H2SO4的作用生成 ClO2和Na2SO4,二氧化氯极易溶于水,用浓硫酸而不用稀硫酸;
(2)装置C中发生气体反应,装置内压强降低,装置B的作用是安全瓶,防止C瓶溶液倒吸到A瓶中,由信息高于38°C时析出晶体是NaClO2可知实验中可采取的措施;
(3)装置C中生成NaClO2,Cl元素的化合价降低,双氧水应表现还原性,有氧气生成,结合原子守恒可知,还有水生成,配平书写方程式;
(4)由题目信息可知,应控制温度38℃~60℃,高于60℃时NaClO2分解成NaClO3和NaCl;
(5)根据化学反应可得关系式:NaClO2~2I2~4S2O32-,根据关系式计算.
解答 解:(1)装置A中产生ClO2,反应的化学方程式为2NaClO3+Na2SO3+H2SO4=2Na2SO4+2ClO2↑+H2O,该装置中采用浓硫酸而不用稀硫酸的原因是减少ClO2溶解,\
故答案为:2NaClO3+Na2SO3+H2SO4=2Na2SO4+2ClO2↑+H2O;减少ClO2溶解;
(2)装置C中发生气体反应,装置内压强降低,装置B的作用是安全瓶,防止C瓶溶液倒吸到A瓶中,装置C反应后的溶液获得NaClO2晶体,根据已知①,给C装置加冰水浴和缓慢滴加硫酸,
故答案为:防止倒吸; 给C装置加冰水浴、缓慢滴加硫酸;
(3)装置C中生成NaClO2,Cl元素的化合价降低,双氧水应表现还原性,有氧气生成,结合原子守恒可知,还有水生成,配平后方程式为:2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2,
故答案为:2ClO2+H2O2+2OH-=2ClO2-+O2↑+2H2O;
(4)从溶液中制取晶体,一般采用蒸发结晶、过滤、洗涤、干燥的方法,为防止析出晶体NaClO2•3H2O,应趁热过滤,由题目信息可知,应控制温度38℃~60℃进行洗涤,低于60℃干燥,
故答案为:趁热过滤;乙醇;低于60℃;
(5)设样品中NaClO2的物质的量x,
NaClO2~2I2~4S2O32-,
1mol 4mol
0.25x c mol•L-1×V×10-3L
则:x=c•V•10-3mol
样品中NaClO2的质量分数为:$\frac{90.5×cv×1{0}^{-3}}{m}$×100%
故答案为:$\frac{90.5×cv×1{0}^{-3}}{m}$×100%.
点评 本题考查物质的制备实验,为高频考点,把握制备实验原理、混合物分离提纯为解答该题的关键,侧重分析与实验能力的考查,注意氧化还原反应的应用,题目难度中等.


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.45mol/L | B. | 0.5mol/L | C. | 0.6mol/L | D. | 0.55mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
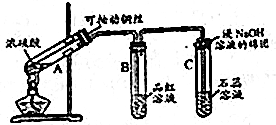
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
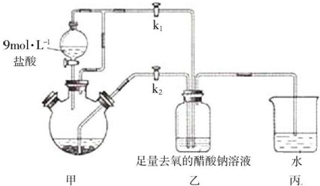
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
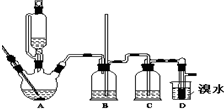 实验室制备1,2二溴乙烷的反应原理如下:
实验室制备1,2二溴乙烷的反应原理如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
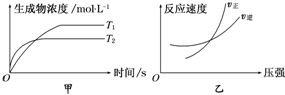
| A. | a+b>c+d T1>T2△H>0 | B. | a+b>c+d T1<T2 △H<0 | ||
| C. | a+b<c+d T1>T2△H>0 | D. | a+b>c+d T1>T2△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2:3 | B. | 3:2:1 | C. | 9:3:1 | D. | 6:3:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com