
”¾ĢāÄæ”æĘ«¶ž¼×ėĀÓėN2O4ŹĒ³£ÓƵĻš¼żĶĘ½ų¼Į£¬¶žÕß·¢ÉśČēĻĀ»Æѧ·“Ó¦£ŗ(CH3)2NNH2(l)+2N2O4(l)£½2CO2(g)+3N2(g)+4H2O(g) (¢ń)
£Ø1£©·“Ó¦(¢ń)ÖŠŃõ»Æ¼ĮŹĒ_________”£
£Ø2£©»š¼ż²Šŗ”ÖŠ³£³öĻÖŗģ×ŲÉ«ĘųĢ壬ŹĒŅņĪŖ£ŗN2O4(g)![]() 2NO2(g)(¢ņ)”£µ±ĪĀ¶ČÉżøߏ±£¬ĘųĢåŃÕÉ«±äÉī£¬Ōņ·“Ó¦(¢ņ)ĪŖ____________(Ģī”°ĪüČČ”±»ņ”°·ÅČČ”±)·“Ó¦”£
2NO2(g)(¢ņ)”£µ±ĪĀ¶ČÉżøߏ±£¬ĘųĢåŃÕÉ«±äÉī£¬Ōņ·“Ó¦(¢ņ)ĪŖ____________(Ģī”°ĪüČČ”±»ņ”°·ÅČČ”±)·“Ó¦”£
£Ø3£©550”ꏱ£¬½«2.0molSO2ŗĶ1.0molO2ÖĆÓŚ5LĆܱÕČŻĘ÷ÖŠ£¬·“Ó¦“ļĘ½ŗāŗó£¬ĻĀĮŠ“ėŹ©ÖŠÄÜŹ¹n(SO3)/n(SO2)Ōö“óµÄŹĒ_____________”£
A.ÉżøßĪĀ¶Č
B.³äČėHe(g)£¬Ź¹ĢåĻµ×ÜŃ¹ĒæŌö“ó
C.ŌŁ³äČė2.0molSO2ŗĶ1.0molO2
”¾“š°ø”æN2O4 ĪüČČ C
”¾½āĪö”æ
(1)ŅŃÖŖŌŚ·“Ó¦ (CH3)2NNH2(l)+2N2O4(l)£½2CO2(g)+3N2(g)+4H2O(g)ÖŠ£¬CŌŖĖŲ“Ó-2¼ŪÉżøßµ½+4¼Ū£¬Ę«¶ž¼×ėĀÖŠµÄNŌŖĖŲ“Ó-2¼ŪÉżøßµ½0¼Ū£¬ĖłŅŌ(CH3)2NNH2×÷»¹Ō¼Į£¬¶ųN2O4ÖŠµÄNŌŖĖŲ“Ó+4¼Ū½µµĶµ½0¼Ū£¬¹ŹN2O4×÷Ńõ»Æ¼Į£»
(2)¶ŌÓŚ·“Ó¦N2O4(g)![]() 2NO2(g)£¬µ±ĪĀ¶ČÉżøߏ±£¬ĘųĢåŃÕÉ«±äÉī£¬ĖµĆ÷·“Ӧɜ³ÉNO2µÄĮæ¶ąĮĖ£¬¼“ÉżĪĀĻņÕżĻņŅĘ¶Æ£¬ŌņøĆ·“Ó¦ĪŖĪüČČ·“Ó¦£»
2NO2(g)£¬µ±ĪĀ¶ČÉżøߏ±£¬ĘųĢåŃÕÉ«±äÉī£¬ĖµĆ÷·“Ӧɜ³ÉNO2µÄĮæ¶ąĮĖ£¬¼“ÉżĪĀĻņÕżĻņŅĘ¶Æ£¬ŌņøĆ·“Ó¦ĪŖĪüČČ·“Ó¦£»
(3)øł¾Ż·“Ó¦·½³ĢŹ½2SO2+ O2 ![]() 2SO3 ¦¤H£¼0”£·ÖĪöČēĻĀ£ŗA”¢ÉżøßĪĀ¶Č£¬Ę½ŗāÄęĻņŅĘ¶Æ£¬Ź¹n(SO3)¼õŠ”£¬n(SO2)Ōö“ó£¬Ōņn(SO3)/n(SO2)ŹĒ¼õŠ”µÄ£¬¹ŹA“ķĪó£»B”¢³äČėHe(g)£¬Ź¹ĢåĻµ×ÜŃ¹ĒæŌö“󣬵«·“Ó¦ĢåĻµµÄ·ÖŃ¹²»±ä£¬ĖłŅŌĘ½ŗā²»ŅĘ¶Æ£¬¹Źn(SO3)/n(SO2)ŹĒ²»±äµÄ£¬B“ķĪó£»C”¢ŌŁ³äČė2.0 mol SO2ŗĶ1.0 mol O2£¬Ļąµ±ÓŚ¼ÓŃ¹£¬ŌņĘ½ŗāÕżĻņŅĘ¶Æ£¬Ź¹n(SO3) Ōö“ó£¬n(SO2) ¼õŠ”£¬Ōņn(SO3)/n(SO2)ŹĒŌö“óµÄ£¬¹ŹCÕżČ·”£±¾ĢāÕżČ·“š°øĪŖC”£
2SO3 ¦¤H£¼0”£·ÖĪöČēĻĀ£ŗA”¢ÉżøßĪĀ¶Č£¬Ę½ŗāÄęĻņŅĘ¶Æ£¬Ź¹n(SO3)¼õŠ”£¬n(SO2)Ōö“ó£¬Ōņn(SO3)/n(SO2)ŹĒ¼õŠ”µÄ£¬¹ŹA“ķĪó£»B”¢³äČėHe(g)£¬Ź¹ĢåĻµ×ÜŃ¹ĒæŌö“󣬵«·“Ó¦ĢåĻµµÄ·ÖŃ¹²»±ä£¬ĖłŅŌĘ½ŗā²»ŅĘ¶Æ£¬¹Źn(SO3)/n(SO2)ŹĒ²»±äµÄ£¬B“ķĪó£»C”¢ŌŁ³äČė2.0 mol SO2ŗĶ1.0 mol O2£¬Ļąµ±ÓŚ¼ÓŃ¹£¬ŌņĘ½ŗāÕżĻņŅĘ¶Æ£¬Ź¹n(SO3) Ōö“ó£¬n(SO2) ¼õŠ”£¬Ōņn(SO3)/n(SO2)ŹĒŌö“óµÄ£¬¹ŹCÕżČ·”£±¾ĢāÕżČ·“š°øĪŖC”£


 ĮĮµć¼¤»ī¾«±ąĢįÓÅ100·Ö“óŹŌ¾ķĻµĮŠ“š°ø
ĮĮµć¼¤»ī¾«±ąĢįÓÅ100·Ö“óŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹµŃéŹŅÓĆČ¼Éշزā¶Øij¹ĢĢåÓŠ»śĪļAµÄ·Ö×Ó×é³É£¬²ā¶Ø×°ÖĆČēĶ¼(Ģś¼ÜĢØ”¢Ģś¼Š”¢¾Ę¾«µĘµČĪ“»³ö)£ŗ

Č”17.1 g A·ÅČė×°ÖĆÖŠ£¬ĶØČė¹żĮæO2Č¼ÉÕ£¬Éś³ÉCO2ŗĶH2O£¬Ēė»Ų“šĻĀĮŠÓŠ¹ŲĪŹĢā£ŗ
(1)ĶØČė¹żĮæO2µÄÄæµÄ______________________”£
(2)C×°ÖƵÄ×÷ÓĆŹĒ_____________________________”£D×°ÖƵÄ×÷ÓĆŹĒ_____________________”£
(3)ĶعżøĆŹµŃ飬ÄÜ·ńČ·¶ØAÖŠŹĒ·ńŗ¬ÓŠŃõŌ×Ó£æ__________”£
(4)ČōAµÄĦ¶ūÖŹĮæĪŖ342 g/mol£¬C×°ÖĆŌöÖŲ9.90 g£¬D×°ÖĆŌöÖŲ26.4 g£¬ŌņAµÄ·Ö×ÓŹ½ĪŖ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æA (C2H4)ŹĒ»ł±¾µÄÓŠ»ś»Æ¹¤ŌĮĻ”£ÓĆAŗĶ³£¼ūµÄÓŠ»śĪļæÉŗĻ³ÉŅ»ÖÖĆŃĄąĻćĮĻŗĶŅ»ÖÖĖõČ©ĄąĻćĮĻ£¬¾ßĢåŗĻ³ÉĀ·ĻßČēĶ¼ĖłŹ¾£Ø²æ·Ö·“Ó¦Ģõ¼žĀŌČ„)£ŗ
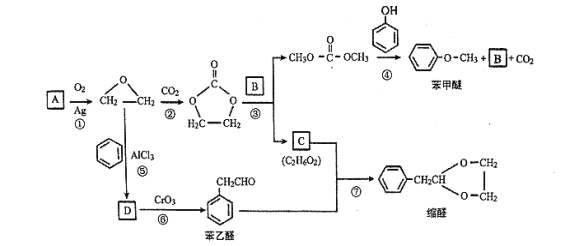
ŅŃÖŖ£ŗ![]()
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©BµÄ·Ö×ÓŹ½ŹĒ_______£¬CÖŠŗ¬ÓŠµÄ¹ŁÄÜĶÅĆū³ĘŹĒ_______”£
£Ø2£©ČōDĪŖµ„Č”“ś·¼Ļć×å»ÆŗĻĪļĒŅÄÜÓė½šŹōÄĘ·“Ó¦£»ĆæøöD·Ö×ÓÖŠÖ»ŗ¬ÓŠ1øöŃõŌ×Ó£¬ DÖŠŃõŌŖĖŲµÄÖŹĮæ·ÖŹżŌ¼ĪŖ13.1%£¬ŌņDµÄ½į¹¹¼ņŹ½ĪŖ_______£¬¢ŽµÄ·“Ó¦ĄąŠĶŹĒ_______”£
£Ø3£©¾Ż±ØµĄ£¬·“Ó¦¢ßŌŚĪ¢²Ø·ųÉäĻĀ£¬ŅŌNaHSO4”¤H2OĪŖ“߻ƼĮ½ųŠŠ£¬ĒėŠ“³ö“Ė·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ_______”£
£Ø4£©ĒėŠ“³öĀś×ćĻĀĮŠĢõ¼žµÄ±½ŅŅČ©µÄĖłÓŠĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½£ŗ_______”£
i .ŗ¬ÓŠ±½»·ŗĶ½į¹¹![]()
ii.ŗĖ“Ź²ÕńĒāĘ×ÓŠ4×é·å£¬ĒŅ·åĆ껿֮±ČĪŖ3 : 2 : 2 : 1
£Ø5£©Čō»ÆŗĻĪļEĪŖ±½¼×ĆѵÄĶ¬ĻµĪļ£¬ĒŅĻą¶Ō·Ö×ÓÖŹĮæ±Č±½¼×ĆŃ“ó14£¬ŌņÄÜŹ¹FeCl3ČÜŅŗĻŌÉ«µÄEµÄĖłÓŠĶ¬·ÖŅģ¹¹Ģå¹²ÓŠ_______ (²»æ¼ĀĒĮ¢ĢåŅģ¹¹)ÖÖ”£
£Ø6£©²ĪÕÕ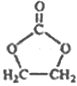 µÄŗĻ³ÉĀ·Ļߣ¬Š“³öÓÉ2-ĀȱūĶéŗĶ±ŲŅŖµÄĪŽ»śŹŌ¼ĮÖʱø
µÄŗĻ³ÉĀ·Ļߣ¬Š“³öÓÉ2-ĀȱūĶéŗĶ±ŲŅŖµÄĪŽ»śŹŌ¼ĮÖʱø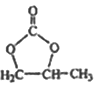 µÄŗĻ³ÉĮ÷³ĢĶ¼£ŗ_______”£
µÄŗĻ³ÉĮ÷³ĢĶ¼£ŗ_______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻņ100mLŗ¬HClµÄAlCl3ČÜŅŗÖŠÖšµĪ¼ÓČė0.1mol”¤L-1µÄNaOHČÜŅŗ£¬¼ÓČėNaOHČÜŅŗµÄĢå»żV£ØmL£©Óė²śÉśAl(OH)3³ĮµķµÄĪļÖŹµÄĮæn£Ømol£©µÄ¹ŲĻµČēĶ¼£ŗ

ŹŌ¼ĘĖć£ŗ£ØĒėŠ“³öŌĖĖć¹ż³Ģ£©
£Ø1£©ŌČÜŅŗÖŠHClµÄĪļÖŹµÄĮæÅØ¶Č”£____________
£Ø2£©ŌČÜŅŗÖŠAlCl3µÄĪļÖŹµÄĮæÅØ¶Č”£____________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗČēĶ¼ÖŠAŹĒ½šŹōĢś£¬Ēėøł¾ŻĶ¼ÖŠĖłŹ¾µÄ×Ŗ»Æ¹ŲĻµ£¬»Ų“šĻĀĮŠĪŹĢā£ŗ

£Ø1£©Š“³öEµÄ»ÆѧŹ½ ____£»
£Ø2£©Š“³ö·“Ó¦¢ŪµÄ»Æѧ·½³ĢŹ½£ŗ__________ £»
£Ø3£©Š“³ö¢Ł¢ÜŌŚČÜŅŗÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ________”¢ ______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æDonepezil(GĪļÖŹ)ŹĒŅ»ÖÖø߶ČŃ”ŌńŠŌµÄŅŅõ£µØ¼īõ„ĆøŅÖÖĘ¼Į£¬ÓĆÓŚÖĪĮĘĒį¶ČŗĶÖŠ¶Č°¢¶ū“Äŗ£Ä¬ŠĶ³Õ“ō֢ד£¬ĖüÄÜĢįøß»¼ÕßµÄČĻÖŖÄÜĮ¦£¬ĘäŗĻ³ÉĀ·ĻßČēĻĀĶ¼ĖłŹ¾(¼żĶ·ÉĻ·½±ķŹ¾·“Ó¦Īļ£¬¼żĶ·ĻĀ·½±ķŹ¾·“Ó¦Ģõ¼ž)£¬Ēė»Ų“šĻą¹ŲĪŹĢā”£
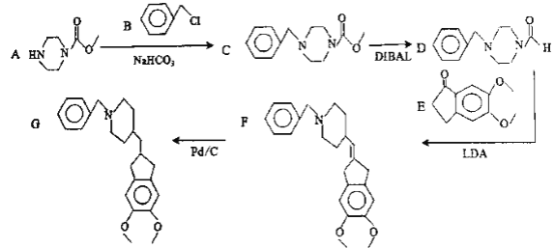
(1)DĪļÖŹµÄ·Ö×ÓŹ½ŹĒ___________£¬EĪļÖŹµÄ¹ŁÄÜĶÅĆū³ĘŹĒ___________”£
(2)F”śGµÄ·“Ó¦ĄąŠĶŹĒ___________”£A”śCµÄ·“Ó¦·½³ĢŹ½ŹĒ______________________”£
(3)BĪļÖŹ·¢ÉśĖ®½ā·“Ó¦µÄĢõ¼žŹĒ___________£¬Ė®½āĖłµĆÓŠ»ś²śĪļµÄĆū³ĘŹĒ___________”£
(4)EĪļÖŹµÄĶ¬·ÖŅģ¹¹ĢåÖŠ·ūŗĻĻĀĮŠŅŖĒóµÄÓŠ___________ÖÖ£¬ĘäÖŠŗĖ“Ź²ÕńĒāĘ×ÖŠ·åµÄŹżÄæ×īÉŁµÄ½į¹¹¼ņŹ½ŹĒ_____________”£
a.·Ö×ÓÖŠŗ¬ÓŠ±½»·
b.±½»·ÉĻÓŠĮ½øöČ”“ś»łĒŅĘäÖŠŅ»øöŹĒ¼×»ł£¬ŗ¬ÓŠōČ»łŗĶČ©»ł
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ½üÄźĄ“”°Īķö²”±ĪŪČ¾ČÕŅęŃĻÖŲ£¬ŌŅņÖ®Ņ»ŹĒ»ś¶Æ³µĪ²ĘųÖŠŗ¬ÓŠNO”¢NO2”¢COµČĘųĢ壬»šĮ¦·¢µē³§ŹĶ·Å³ö“óĮæµÄNOx”¢SO2ŗĶCO2µČĘųĢåŅ²ŹĒĘäŌŅņ£¬ĻÖŌŚ¶ŌĘäÖŠµÄŅ»Š©ĘųĢå½ųŠŠĮĖŅ»¶ØµÄŃŠ¾æ£ŗ
£Ø1£©ÓĆ CH4“߻ƻ¹ŌµŖŃõ»ÆĪļæÉŅŌĻū³żµŖŃõ»ÆĪļµÄĪŪČ¾”£
ŅŃÖŖ£ŗ¢ŁCH4(g) + 4NO2(g) = 4NO(g) + CO2(g) + 2H2O(g) ”÷H = - 574 kJ/mol
¢ŚCH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g) ”÷H = - 1160 kJ/mol
¢ŪH2O(g) = H2O(l) ”÷H = - 44.0 kJ/mol
Š“³ö CH4(g)Óė NO2(g)·“Ӧɜ³É N2(g)”¢CO2(g)ŗĶ H2O(l)µÄČČ»Æѧ·½³ĢŹ½£ŗ _____________________________________________________________”£
£Ø2£©Ęū³µĪ²ĘųÖŠŗ¬ÓŠCO”¢NO2µČÓŠ¶¾ĘųĢ壬¶ŌĘū³µ¼Ó×°Ī²Ęų¾»»Æ×°ÖĆ£¬æÉŹ¹ÓŠ¶¾ĘųĢå×Ŗ»ÆĪŖĪŽ¶¾ĘųĢ唣4CO(g)£«2NO2(g) ![]() 4CO2(g)£«N2(g) ¦¤H£½-1200 kJ”¤mol-1
4CO2(g)£«N2(g) ¦¤H£½-1200 kJ”¤mol-1
¶ŌÓŚøĆ·“Ó¦£¬ĪĀ¶Č²»Ķ¬£ØT2£¾T1£©”¢ĘäĖūĢõ¼žĻąĶ¬Ź±£¬ĻĀĮŠĶ¼ĻńÕżČ·µÄŹĒ________________£ØĢī“śŗÅ£©”£

£Ø3£©ÓĆ»īŠŌĢ滹Ō·ØŅ²æÉŅŌ“¦ĄķµŖŃõ»ÆĪļ£¬Ä³ŃŠ¾æŠ”×éĻņijĆܱÕČŻĘ÷¼ÓČėŅ»¶ØĮæµÄ»īŠŌĢæŗĶNO£¬·¢Éś·“Ó¦C(s)+2NO(g) ![]() N2(g)+CO2(g) ¦¤H=a kJ/mol
N2(g)+CO2(g) ¦¤H=a kJ/mol
ŌŚT1”ꏱ£¬·“Ó¦½ųŠŠµ½²»Ķ¬Ź±¼ä²āµĆø÷ĪļÖŹµÄĮæÅضČČēĻĀ£ŗ
Ź±¼ä/min ÅضČ/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
¢Łøł¾ŻĶ¼±ķŹż¾Ż·ÖĪöT1”ꏱ£¬øĆ·“Ó¦ŌŚ0-20minµÄĘ½¾ł·“Ó¦ĖŁĀŹv£ØNO£©=_____________________£»¼ĘĖćøĆ·“Ó¦µÄĘ½ŗā³£ŹżK=____________________”£
¢Ś30minŗó£¬Ö»øıäijŅ»Ģõ¼ž£¬øł¾ŻÉĻ±ķµÄŹż¾ŻÅŠ¶ĻøıäµÄĢõ¼žæÉÄÜŹĒ_________£ØĢī×ÖÄø“śŗÅ£©”£
A£®ĶØČėŅ»¶ØĮæµÄCO2 B£®¼ÓČėŗĻŹŹµÄ“߻ƼĮ
C£®ŹŹµ±ĖõŠ”ČŻĘ÷µÄĢå»ż D£®ĶØČėŅ»¶ØĮæµÄNO
E£®¼ÓČėŅ»¶ØĮæµÄ»īŠŌĢæ
¢ŪČō30minŗóÉżøßĪĀ¶ČÖĮT2”ę£¬“ļµ½Ę½ŗāŹ±£¬ČŻĘ÷ÖŠNO”¢N2”¢CO2µÄÅضČÖ®±ČĪŖ2:1:1£¬Ōņ“ļµ½ŠĀĘ½ŗāŹ±NOµÄ×Ŗ»ÆĀŹ____________£ØĢī”°Éżøß”±»ņ”°½µµĶ”±£©£¬a________0£ØĢī”°>”±»ņ”°<”±£©”£
£Ø4£©ĪĀ¶ČT1ŗĶT2Ź±£¬·Ö±š½«0.50 mol CH4ŗĶ1.2mol NO2³äČė1 LµÄĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦£ŗCH4(g)£«2NO2(g)![]() N2(g)£«CO2(g)£«2H2O(g) ”÷H=bkJ/mol”£
N2(g)£«CO2(g)£«2H2O(g) ”÷H=bkJ/mol”£
²āµĆÓŠ¹ŲŹż¾ŻČēĻĀ±ķ£ŗ
ĪĀ¶Č | Ź±¼ä/min ĪļÖŹµÄĮæ | 0 | 10 | 20 | 40 | 50 |
T1 | n£ØCH4£©/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n£ØCH4£©/mol | 0.50 | 0.30 | 0.18 | x | 0.15 |
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ__________________”£
A£®T1£¾T2£¬ĒŅb£¾0
B£®µ±ĪĀ¶ČĪŖT2”¢·“Ó¦½ųŠŠµ½40 minŹ±£¬ x£¾0.15
C£®ĪĀ¶ČĪŖT2Ź±£¬ČōĻņĘ½ŗāŗóµÄČŻĘ÷ÖŠŌŁ³äČė0.50 mol CH4ŗĶ1.2mol NO2£¬ÖŲŠĀ“ļµ½Ę½ŗāŹ±£¬n£ØN2£©<0.70mol
D£®ĪĀ¶ČĪŖT1Ź±£¬ČōĘšŹ¼Ź±ĻņČŻĘ÷ÖŠ³äČė0.50 mol CH4(g)”¢0.50 molNO2(g)”¢1.0 mol N2(g)”¢2.0 molCO2(g)”¢0.50molH2O(g)£¬·“Ó¦æŖŹ¼Ź±£¬¦Ķ(Õż)£¾¦Ķ(Äę)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĶ¬Ń§Č”Čż·ŻŠæĮ££¬·ÅČėČżÖ»ÉÕ±ÖŠ£¬Č»ŗóŌŚ¼×”¢ŅŅĮ½Ö»ÉÕ±ÖŠ·Ö±š¼ÓČė2mol/LµÄŃĪĖį”¢Ļ”ĮņĖįø÷45mL£¬±ūÉÕ±ÖŠ¼ÓČėøÕøÕÓĆ5mL18mol/LµÄÅØĮņĖįĻ”ŹĶ¶ų³ÉµÄ45mLĻ”ĮņĖįČÜŅŗ£¬Čō·“Ó¦ÖÕÖ¹Ź±£¬Éś³ÉµÄĘųĢåŅ»Ńł¶ą£¬ĒŅŠæĮ£Ć»ÓŠŹ£Óą”£
£Ø1£©²Ī¼Ó·“Ó¦µÄŠæµÄÖŹĮæ£ŗ¼×___________ŅŅ_________±ū£ØĢī”°>”±”¢”°<”±”¢”°=”±£¬ĻĀĶ¬£©”£
£Ø2£©·“Ó¦ĖŁĀŹ£¬¼×__________ŅŅ£¬ŌŅņŹĒ___________”£
£Ø3£©·“Ó¦Ķź±Ļ ĖłŠčŹ±¼ä£ŗŅŅ____________±ū£¬ŌŅņŹĒ__________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫H2SŗĶæÕĘųµÄ»ģŗĻĘųĢåĶØČėFeCl3”¢FeCl2”¢CuCl2µÄ»ģŗĻČÜŅŗÖŠ·“Ó¦»ŲŹÕS£¬ĘäĪļÖŹ×Ŗ»ÆČēĶ¼ĖłŹ¾”£

£Ø1£©Š“³öCuCl2ÓėH2S·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ_____”£
£Ø2£©ĶعżÉĻŹöĮ÷³ĢĶ¼µÄ·ÖĪö£¬ÕūøöĮ÷³ĢµÄ×Ü·“Ó¦ĪŖ____”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com