
硫代硫酸钠溶液与稀硫酸的反应方程式为:
Na2S2O3+H2SO4====Na2SO4+S↓+SO2+H2O,
某实验兴趣小组用如图所示的实验装置探究外界条件对化学反应速率的影响(加热仪器和夹持仪器均已省略)。
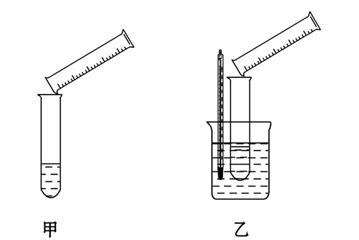
(1)实验目的:装置甲,探究浓度对化学反应速率的影响;装置乙,探究______对化学反应速率的影响。
( 2)通过甲、乙装置,
2)通过甲、乙装置, 分别进行了三组实验,数据记录如下,并经分析得出相关结论:
分别进行了三组实验,数据记录如下,并经分析得出相关结论:
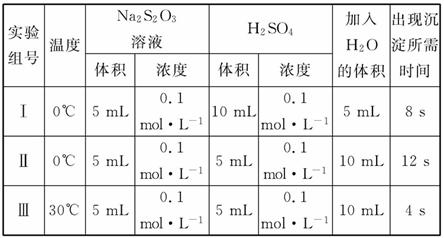
结论1:由Ⅰ和Ⅱ两组数据可知______________________________________;
结论2:由Ⅱ和Ⅲ两组数据可知______________________________________。
(1)在乙图的烧杯中插有温度计,故应该是探究温度对化学反应速率的影响。
(2)由Ⅰ和Ⅱ两组数据可知,Ⅰ和Ⅱ两组实验中反应物Na2S2O3溶液和H2SO4溶液的浓度都相等,再分别加入5 mL、10 mL水后,第Ⅰ组反应物的浓度较大,反应速率较快,因此由Ⅰ和Ⅱ两组数据可知,其他条件一定时,反应物浓度越大,化学反应速率越快。
而从Ⅱ和Ⅲ两组数据可知,Ⅱ和Ⅲ两组实验中反应物Na2S2O3溶液和H2SO4溶液的浓度都相等,加入水的量也相同,故反应物的 浓度两者相等,但第Ⅲ组温度较高,反应速率较快,因此由Ⅱ和Ⅲ两组数据可知其他条件一定时,温度越高,化学反应速率越快。
浓度两者相等,但第Ⅲ组温度较高,反应速率较快,因此由Ⅱ和Ⅲ两组数据可知其他条件一定时,温度越高,化学反应速率越快。
答案:(1)温度
(2)其他条件一定时,反应物浓度越大,化学反应速率越快
其他条件一定时,温度越高,化学反应速率越快


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
①用一种试剂将下列各组物质鉴别开.
(1) 和
和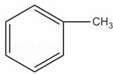 :
:
(2) ,
, 和C6H12(已烯):
和C6H12(已烯):
(3)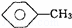 ,CCl4和乙醇
,CCl4和乙醇
②填写
(1)CH3COOC2H5中含有官能团的名称:
(2)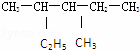 的系统命名:
的系统命名:
(3)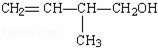 的键线式: .
的键线式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
把下列四种X溶液分别加入四个盛有10 mL 2 mol·L-1盐酸的烧杯中,均加水稀释到50 mL,此时,X和盐酸缓慢地进行反应,其中反应最快的是( )
A.10 ℃ 20 mL 3 mol·L-1的X溶液
B.20 ℃ 30 mL 2 mol·L-1的X溶液
C.20 ℃ 10 mL 4 mol·L-1的X溶液
D.10 ℃ 10 mL 2 mol·L-1的X溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
“玉兔”号月球车用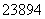 Pu作为热源材料,下列关于
Pu作为热源材料,下列关于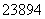 Pu的说法正确的是( )
Pu的说法正确的是( )
A.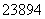 Pu与
Pu与 U互为同位素
U互为同位素
B.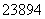 Pu与
Pu与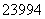 Pu互为同素异形体
Pu互为同素异形体
C.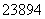 Pu与
Pu与 U具有完全相同的化学性质
U具有完全相同的化学性质
D.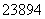 Pu与
Pu与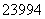 Pu具有相同的最外层电子
Pu具有相同的最外层电子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学键的叙述,正确的一项是( )
A.离子化合物中一定含有离子键
B.单质分子中均不存在化学键
C.非金属元素组成的化合物中只含共价键
D.含有共价键的化合物一定是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y 处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是( )
A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大
B.元素X不能与元素Y形成化合物X2Y2
C.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR
D.元素W、R的最高价氧化物的水化物都是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
设阿伏加德罗常数的数值约为6.02×1023,下列叙述中正确的是( )
A.0.5 g C3H4中含有共用电子对的数目为0.1×6.02×1023
B.3.0 g淀粉和葡萄糖混合物中共含碳原子数为0.1×6.02×1023
C.25℃时,pH=1的醋酸溶液中含有H+的数目为0.1×6.02×1023
D.标准状况下,2.24 L CHCl3中含有的分子数为0.1×6.02×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com