
分析 (1)取20.00mL硫酸亚铁铵溶液于锥形瓶,用0.1000mol•L-1的酸性KMnO4溶液进行滴定发生反应为高锰酸钾溶液氧化亚铁离子为铁离子,结合电荷守恒和原子守恒书写离子方程式,利用高锰酸钾溶液的颜色变化判断反应终点;
(2)取20.00mL硫酸亚铁铵溶液加入氯化钡溶液生成硫酸钡沉淀,测定沉淀质量计算,亚铁离子具有还原性,易被氧化;检验亚铁离子的氧化产物铁离子;
(3)①根据氨气的溶解性和装置特点分析;
②根据氨气的体积计算氨气的物质的量,根据N守恒计算出硫酸亚铁铵的质量,进而计算质量分数.
解答 解:(1)酸性KMnO4溶液进行滴定发生反应时高锰酸钾溶液氧化亚铁离子为铁离子,反应的离子方程式为5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,判断达到滴定终点的依据是当最后一滴酸性高锰酸钾标准溶液滴入时,锥形瓶内溶液由黄色变为浅紫色,且半分钟内不再恢复原色,说明达到滴定终点,
故答案为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;当最后一滴酸性高锰酸钾标准溶液滴入时,锥形瓶内溶液由黄色变为浅紫色,且半分钟内不再恢复原色,说明达到滴定终点;
(2)取20.00mL硫酸亚铁铵溶液加入氯化钡溶液生成硫酸钡沉淀,反应的离子方程式为:SO42-+Ba2+=BaSO4↓,亚铁离子具有还原性,易被氧化成铁离子,故测得硫酸亚铁铵浓度偏小;可检验亚铁离子的氧化产物铁离子,具体操作为:取少量硫酸亚铁铵溶液,加入少量KSCN溶液,若溶液变为血红色,说明Fe2+已被空气部分氧化;
故答案为:SO42-+Ba2+=BaSO4↓;Fe2+已被空气部分氧化;取少量硫酸亚铁铵溶液,加入少量KSCN溶液,若溶液变为血红色,说明Fe2+已被空气部分氧化;
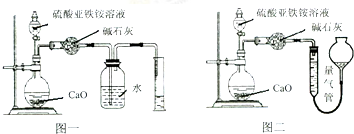
(3)①氨气易溶于水,不能用排水法收集,图一装置中导管伸入液面下,易倒吸,用排水法,不合理;图二装置中导管在液面以上,符合排液体收集气体要求,量气管中液体应不能溶解氨气,氨气易溶于水和饱和碳酸钠溶液,难溶于四氯化碳,故用排四氯化碳法收集;
故答案为:图二;氨气极易溶于水,图一装置无法排液体,甚至会出现倒吸;c;
②VL氨气的物质的量为:$\frac{VL}{22.4L/mol}$=$\frac{V}{22.4}$mol,m g硫酸亚铁铵样品中含N的物质的量为$\frac{500ml}{20ml}$×$\frac{V}{22.4}$mol=$\frac{25V}{22.4}$mol,
硫酸亚铁铵的纯度为:$\frac{\frac{25V}{22.4}mol×\frac{1}{2}×392g/mol}{mg}$×100%=$\frac{392V×500}{2×22.4m×20}$×100%,
故答案为:$\frac{392V×500}{2×22.4m×20}$×100%.
点评 本题考查制备实验方案的设计,综合性较强,注意结合题给信息和装置特点及物质的性质分析.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | Y的最高价氧化物对应水化物的酸性比W的强 | |
| B. | W的气态氢化物比X的稳定 | |
| C. | 离子半径的大小顺序:r(W)>r(X)>r(Y)>r(Z) | |
| D. | WX2与ZY2中的化学键类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的 | |
| B. | 在船底镶嵌锌块和将船体与电源负极相连,二者防腐的方法都称为牺牲阳极的阴极保护法 | |
| C. | 1 mol葡萄糖水解能生成2mol CH3CH2OH和2mol CO2 | |
| D. | 不能用带玻璃塞的玻璃瓶和酸式滴定管盛取碱液,二者的原因是相同的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 结论 |
| 在“褐变”后的苹果上滴上2~3滴 KSCN溶液. | 无红色出现 | 说法A不正确 |
| 序号 | 实验步骤 | 现 象 | 结 论 |
| ① | 在一块上滴加2~3滴FeCl3溶液 | 表面变为绿色 | 对苯二酚 |
| ② | 再取两块,一块放置于空气中,另一块迅速浸入经过去氧的蒸馏水中. | 前者表面逐渐褐变,后者相当长一段时间内,无明显变化. | 苹果褐变与氧气有关 |
| ③ | 另两块分别立刻放入沸水和0.1mol•L-1盐酸中浸泡2min后取出,置于空气中. | 相当长一段时间内,两块均无明显变化. | 苹果褐变与酚氧化酶的活性有关 |
| ④ | 最后两块分别立刻放入浓度均为0.1mol•L-1的NaHCO3和Na2SO3溶液里浸泡2min后取出,置于空气中. | 前者经过一段时间表面逐渐褐变,后者相当长一段时间内,无明显变化. | 亚硫酸钠溶液能阻止苹果褐变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二甲苯和四甲苯均有三种 | |
| B. | 乙醇的酯化反应和酯的水解均属于取代反应 | |
| C. | 乙醇、乙酸均可与金属钠反应 | |
| D. | 石油裂解和油脂皂化均是由高分子物质生成小分子物质的过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质的还原性:W>X>Y | |
| B. | 原子半径:X>Y>Z>W | |
| C. | X的最高价氧化物对应水化物的碱性比Y的弱 | |
| D. | 化合物XYW4具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
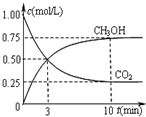 工业上可以以煤和水为原料通过一系列转化变为清洁能源氢气或工业原料甲醇.
工业上可以以煤和水为原料通过一系列转化变为清洁能源氢气或工业原料甲醇.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com