
下列有关实验操作的说法正确的是
A.可用25ml碱式滴定管量取20.00 ml KMnO4 溶液
B.用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
C.用量筒量取5.00 mL 1. 00mol·L-1盐酸于50mL容量瓶中,加水稀释至刻度可配
制0.100mol·L-1盐酸
D.中和滴定时盛待测液的锥形瓶中有少量水对滴定结果无影响
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.滴入酚酞溶液显红色的溶液中:K+、Na+、Cu2+、SO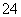
B.加入过量NaOH溶液或少量稀H2SO4时,都能产生白色沉淀的溶液:K+、Ba2+、Cl-、HCO
C.水电离产生的c(H+)=10-13 mol·L-1的溶液中:Na+、Cl-、NO 、CH3COO-
、CH3COO-
D.pH=1的溶液中:Na+、NO 、S2-、Cl-
、S2-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
对金属制品进行抗腐蚀处理,可延长其使用寿命。
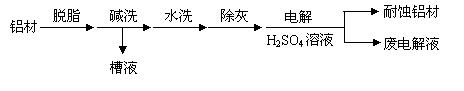 (1)以下为铝材表面处理的一种方法:
(1)以下为铝材表面处理的一种方法:
① 碱洗的目的是除去铝材表面的自然氧化膜,为将碱洗槽液中铝以沉淀形式回收,最好向槽液中加入下列试剂中的 。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4 溶液中电解,铝材表面形成氧化膜,阳极电极反应为
。取少量废电解液,加入NaHCO3,溶液后产生气泡和白色沉淀,产生沉淀的原因是 。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是 。
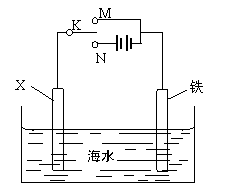
(3)利用下图装置,可以模拟铁的电化学防护。
若X为碳棒,为减缓铁的腐蚀,开关K应置于 处。若X为锌,开关K置于 处。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是
A.强电解质溶液的导电能力一定比弱电解质溶液的强
B.离子化合物中可能有共价键,共价化合物中肯定没有离子键
C.强电解质都是可溶性化合物,弱电解质都是难溶性化合物
D.NaCl晶体不导电是由于NaCl晶体中不存在离子
查看答案和解析>>
科目:高中化学 来源: 题型:
常温条件下,下列各组离子在指定溶液中能大量共存的是
A.使石蕊试液变红的溶液中:Fe2+、NO 、SO42—、Na+
、SO42—、Na+
B.由水电离出的c(H+)=1×10-14mol/L的溶液中:Ca2+、Cl-、HCO 、K+
、K+
C.c(H+)/c(OH-)=1×1012的溶液中:NH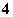 、Cl-、SO42—、Al3+
、Cl-、SO42—、Al3+
D.c(Al3+)=0.1 mol/L的溶液中:K+、Cl-、SO42—、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在5 mL 0.1 mol/L的KCl溶液中,加入5 mL 0.1 mol/L的AgNO3溶液,可观察到____________,此反应的离子方程式为_____________________。
将此混合液过滤,滤渣加入5 mL 0.1 mol/L的KI溶液,搅拌,可观察到________________________,反应的离子方程式为_____________________。
(2)对于Ag2S(s) 2Ag+(aq)+S2-(aq),其Ksp的表达式为_____________________。
2Ag+(aq)+S2-(aq),其Ksp的表达式为_____________________。
(3)下列说法不正确的是________。
A.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小
B.对于Al(OH)3(s)  Al(OH)3(aq)
Al(OH)3(aq)  Al3++3OH-,前者为溶解平衡,后者为电离平衡
Al3++3OH-,前者为溶解平衡,后者为电离平衡
C.物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的
D.沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全
E.用OH-除去溶液中的Mg2+比用CO 效果好,说明Mg(OH)2的溶解度比MgCO3大
效果好,说明Mg(OH)2的溶解度比MgCO3大
(4)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是______。
A. KMnO4 B. H2O2 C. Cl2 水 D. HNO3
然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的________。
A. NaOH B. NH3·H2O C. CuO D. Cu(OH)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com