
【题目】一定量混合物在密闭容器中发生反应:mA(g)+nB(g)![]() pC(g)达平衡后,将气体体积缩小到原来的1/2,当达到新的平衡时,B物质的浓度为原来的1.9倍,若压缩过程中保持温度不变,则下列说法正确的是
pC(g)达平衡后,将气体体积缩小到原来的1/2,当达到新的平衡时,B物质的浓度为原来的1.9倍,若压缩过程中保持温度不变,则下列说法正确的是
A.m+n<pB.平衡向逆反应方向移动C.A的转化率降低D.C的体积分数增大
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:
【题目】过氧化钙晶体(CaO2·8H2O)常用作医药消毒剂,可以轻质碳酸钙为原料,按以下实验方法来制备。
![]()
下列有关说法正确的是
A. ①煮沸的主要目的是为了除去溶解的CO2
B. ②的反应中H2O2作氧化剂,氨水用来调节溶液的pH
C. ②中结晶的颗粒较小,过滤时可用玻璃棒轻轻搅动
D. ③醇洗的主要目的是为了减少晶体的损失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可在高纯度氨气下,通过球磨氢化锂的方式合成高纯度的储氢材料氨基锂,该过程中发生反应:LiH(s)+NH3(g)=LiNH2(s)+H2 (g)。如图表示在0.3 MPa下,不同球磨时间的目标产物LiNH2的相对纯度变化曲线。下列说法正确的是 ( )
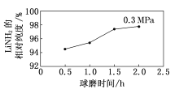
A.工业生产中,在0.3 MPa下合成LiNH2的最佳球磨时间是2.0 h
B.投入定量的反应物,平衡时混合气体的平均摩尔质量越大,LiNH2的相对纯度越高
C.在0.3 MPa下,若平衡时H2的物质的量分数为60%,则该反应的平衡常数K=1.5
D.LiH和LiNH2都能在水溶液中稳定存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用合成EPR橡胶![]() 的两种单体A和B合成PC塑料
的两种单体A和B合成PC塑料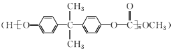 其合成路线如下:
其合成路线如下:
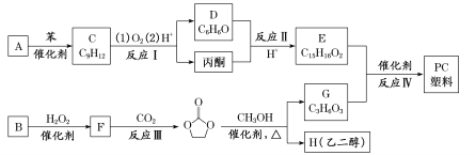
已知:①RCOOR1+R2OH![]() RCOOR2+R1OH
RCOOR2+R1OH
②(CH3)2C=CHCH3+H2O2![]()
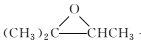 +H2O
+H2O
③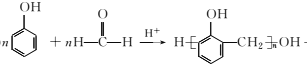 +(n-1)H2O
+(n-1)H2O
回答下列问题:
(I)F的结构简式为__________,反应Ⅲ的反应类型为___________。
(2)C的名称为__________。
(3)写出反应Ⅳ的化学方程式:____________________。
(4)从下列选项中选择______试剂,可以一次性鉴别开D、G、H三种物质。(填字母)
A.氯化铁溶液 B.浓溴水 C.酸性KMnO4溶液
(5)满足下列条件的有机物E的同分异构体有__________种。
①与E属于同类别物质;②核磁共振氢谱有6组峰,峰面积比为1:1:1:1:1:3。
(6)以丙烯和丙酮为原料合成![]() ,无机试剂任选,写出合成路线__________________________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
,无机试剂任选,写出合成路线__________________________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语的相关表述中正确的是
A. 因H+(aq) +OH- (aq)==H2O(l) △H=-akJ·mol-1,故1molNaOH固体与足量的稀盐酸反应,放出的热量为akJ
B. 因CuSO4·5H2O(s)==CuSO4(s)+5H2O(1)△H=+bkJ·mol-1,故1molCuSO4(s)溶于水时,放出的热量为bkJ
C. 因氢气的燃烧热为c kJ·mol-1,故水电解的热化学方程式为2H2O (l)==2H2(g)+O2(g) △H=+c kJ·mol-1
D. 因N2(g)+3H2(g)![]() 2NH3(g) △H=-d kJ·mol-1,故在某容器中通入1molN2与3molH2充分反应后,放出的热量小于dkJ
2NH3(g) △H=-d kJ·mol-1,故在某容器中通入1molN2与3molH2充分反应后,放出的热量小于dkJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向FeBr2溶液中通入适量Cl2,溶液由浅绿色变为黄色 | Cl2氧化性强于Br2 |
B | 常温下,等体积pH=3的HA和HB两种酸分别加水稀释,溶液导电能力如图
| HA酸性比HB弱 |
C | 向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀 | X具有氧化性 |
D | 取久置的Na2O2粉末,向其中滴加过量的盐酸,产生无色气体 | 气体为氧气 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白。
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视____,直到因加入一滴盐酸后,溶液由______色变为____色,并____为止。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是__________。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则起始读数为_____mL,所用盐酸溶液的体积为_____mL。

(4)某学生根据3次实验分别记录有关数据如表:
滴定 次数 | 待测NaOH溶液的体积/mL | 0.1000mol·L-1盐酸的体积/mL | ||
滴定前读数 | 滴定后读数 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 25.11 | 25.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 25.31 | 25.09 |
依据表中数据列式计算该NaOH溶液的物质的量浓度_____(保留两位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分是![]() ,含
,含![]() 、
、![]() 、MgO等杂质)中提取两种工艺品的流程如下:
、MgO等杂质)中提取两种工艺品的流程如下:

请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的方程式为_________.
(2)流程乙加入烧碱后生成SiO32-的离子方程式为________.
(3)验证滤液B含![]() ,可取少量滤液并加入________(填试剂名称)。
,可取少量滤液并加入________(填试剂名称)。
(4)滤液E、K中溶质的主要成份是________(填化学式),写出该溶液的一种用途________
(5)已知298K时,![]() 的容度积常数
的容度积常数![]() =5.6×
=5.6×![]() ,取适量的滤液B,加入一定量的烧碱达到沉淀溶液平衡,测得PH=13.00,则此温度下残留在溶液中的
,取适量的滤液B,加入一定量的烧碱达到沉淀溶液平衡,测得PH=13.00,则此温度下残留在溶液中的![]() =_______.
=_______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I2在KI溶液中存在下列平衡:I2(aq) + I-(aq) ![]() I3-(aq)。某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是
I3-(aq)。某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是
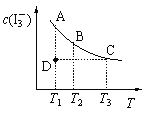
A.反应 I2(aq) + I-(aq) ![]() I3-(aq)的△H>0
I3-(aq)的△H>0
B.状态A与状态B相比,状态A的c(I2)大
C.若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1<K2
D.若反应进行到状态D时,一定有v正>v逆
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com