
常温下,对pH=10的NaHCO3溶液中,各微粒的物质的量浓度分析正确的是( )
A.c(CO32—)>c(H2CO3)
B.c(Na+)>c(HCO3—)>c(OH—)>c(H+)
C.c(Na+)+c(H+)=c(HCO3—)+c(CO32—)+c(OH—)
D.c(Na+)=c(HCO3—)+c(CO32—)
【知识点】溶液中的离子浓度关系H3 H6
【答案解析】B 解析:A、HCO3-+H2O H2CO3+OH-;HCO3-
H2CO3+OH-;HCO3- H++CO32-,NaHCO3溶液显碱性,说明HCO3-的水解程度大于电离程度,所以c(H2CO3)>c(CO32—),故A错误;B、因HCO3-的水解,c(Na+)>c(HCO3—),NaHCO3溶液显碱性c(OH—)>c(H+),故B正确;C、根据电荷守恒,正确的关系是:c(Na+)+c(H+)=c(HCO3—)+2c(CO32—)+c(OH—),故C错误;D、根据物料守恒:c(Na+)=c(HCO3—)+c(CO32—)+c(H2CO3),故D错误。
H++CO32-,NaHCO3溶液显碱性,说明HCO3-的水解程度大于电离程度,所以c(H2CO3)>c(CO32—),故A错误;B、因HCO3-的水解,c(Na+)>c(HCO3—),NaHCO3溶液显碱性c(OH—)>c(H+),故B正确;C、根据电荷守恒,正确的关系是:c(Na+)+c(H+)=c(HCO3—)+2c(CO32—)+c(OH—),故C错误;D、根据物料守恒:c(Na+)=c(HCO3—)+c(CO32—)+c(H2CO3),故D错误。
故答案选B
【思路点拨】本题考查了溶液中的离子浓度关系,理解电荷守恒、物料守恒、元素守恒是关键。


 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
下列物质的转化在给定条件下能实现的是( )
①SO2 H2SO3
H2SO3 H2SO4 ②NH3
H2SO4 ②NH3 NO2
NO2 HNO3 ③CaCl2
HNO3 ③CaCl2 CaCO3
CaCO3 CaO
CaO
④NaAlO2(aq) Al(OH)3
Al(OH)3 Al2O3
Al2O3
A.②③ B.①④ C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
在常压和500 ℃条件下,等物质的量的Ag2O、Fe(OH)3、NH4HCO3、NaHCO3完全分解,所得气体体积依次为V1、V2、V3、V4。体积大小顺序正确的是( )
A.V3>V2>V4>V1 B.V3>V4>V2>V1
C.V3>V2>V1>V4 D.V2>V3>V1>V4
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:95℃时,KW=1.0×10-12.在该温度下,测得0.1mol·L-1Na2A溶液PH=6,则下列说法正确的是
A.H2A在水溶液中的电离方程式为:H2A  H++HA-,HA-
H++HA-,HA-  H++A2-
H++A2-
B.(NH4)2A溶液中存在离子浓度关系:c(NH4+)>c(A2-)>c(H+)>c(OH-)
C.0.0lmol·L-l的H2A溶液pH=2
D.等体积等浓度的盐酸与H2A溶液分别与5.6g Zn反应,H2A溶液产生的H2多
查看答案和解析>>
科目:高中化学 来源: 题型:
对下列各溶液中,微粒的物质的量浓度关系表述正确的是
A.0.1mol·L-1的(NH4)2CO3溶液中:c(CO32-)>c(NH4+)>c(H+)>c(OH-)
B. 0.1 mol·L-1的NaHCO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+2c(CO32-)
C.将0.2 mol·L-1 NaA溶液和0.1 mol·L-1盐酸等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-)
D.在25℃时,1mol·L-1的CH3COONa溶液中:c(OH-)=c(H+)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列图示与对应的叙述不相符的是( )
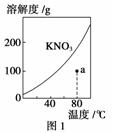

A.图1表示KNO3的溶解度曲线,图中a点所示的溶液是80 ℃时KNO3的不饱和溶液
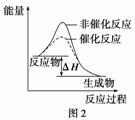
B.图2表示某放热反应分别在有、无催化剂的情况下反应过程中的 能量变化
能量变化
C.图3表示0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1醋酸溶液得到的滴定曲线
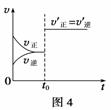
D.图4表示已达平衡的某反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件可能是增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,PbO2与Cr3+反应,产物是Cr2O72—和 Pb2+,则与1molCr3+反应所需PbO2的物质的量为( )
A.3.0 mol B.1.5mol C.1.0mol D.0.75mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com