
具有下列特征的原子,一定是非金属元素的是( )
A、最外层电子数大于4
B、具有负化合价
C、最高价氧化物对应的水化物只是酸
D、具有可变化合价
科目:高中化学 来源: 题型:
β紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素A1。
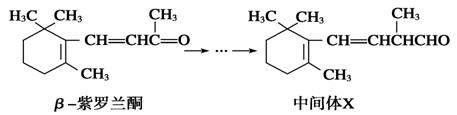
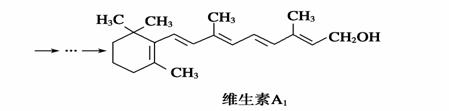
下列说法正确的是 ( )
A.维生素A1易溶于NaOH溶液
B.1 mol中间体X最多能与2 mol H2发生加成反应
C.β紫罗兰酮可使酸性KMnO4溶液褪色
D.β紫罗兰酮与中间体X互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
若NA是阿伏加德罗常数的值,下列说法不正确的是( )
A.1 mol Cl2与足量的铁反应,转移电子数为3NA
B.7.8 g Na2O2含有的阴离子数为0.1NA
C.标准状况下,2.24 L丁烷分子所含的C—H键数为NA
D.5.6 g CO和N2组成的混合气体所含的质子数为2.8NA
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组欲测定室温下(25℃、101 kPa)的气体摩尔体积,请回答以下问题。
该小组设计的简易实验装置 如图所示:
如图所示:

该实验的主要操作步骤如下:
①配制100 mL 1.0 mol/L 的盐酸溶液;
②用__________(填仪器名称并注明规格)量取10.0 mL 1.0 mol/L 的盐酸溶液加入锥形瓶中;
③称取a g 已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为________;
④往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为V mL。
请将上述步骤补充完整并回答下列问题。
(1)用文字表述实验步骤④中检查装置气密性的方法:
________________________________________________________________________
________________________________________________________________________。
(2)实验步骤⑤中应选用________(填序号)的量筒。
A.100 mL B.200 mL C.500 mL
读数时除恢复到室温外,还要注意_________________________________________。
(3)若忽略水蒸气的影响,在实验条件下测得气体摩尔体积的计算式为Vm=________,若未除去镁条表面的氧化膜,则测量结果________(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据以下事实得出的判断一定正确的是( )
A、HA的酸性比HB的强,则HA溶液的pH比HB溶液的小
B、A+和B-的电子层结构相同,则A原子的核电荷数比B原子的大
C、A盐的溶解度在同温下比B盐的大,则A盐溶液的溶质质量分数比B盐溶液的大
D、A原子失去的电子比B原子的多,则A单质的还原性比B单质的强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关叙述正确的是( )
A、元素的化学性质随着相对原子质量的递增而呈周期性变化
B、元素周期律的实质是因为元素原子最外层电子数由1→8周期性变化而引起的
C、半径由大到小、氧化性由弱到强的是:K+、Mg2+、Al3+、H+,而还原性由弱到强的则是:I-、Br-、Cl-、F-
D、某元素R的最高价氧化物化学式为:R2O5,又知R的气态氢化物中含氢的质量分数为8.8%,则R的相对原子质量为28
查看答案和解析>>
科目:高中化学 来源: 题型:
元素氟位于周期表右上角,下列对元素氟的相关叙述正确的是( )
A、还原性:F—>Br— B、酸性:HF>HCl C、稳定性:HF<HCl D.半径:F<Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
右图是元素周期表短周期的一部分,A、B两种元素可以形成共价化合物B2A2,分子中所有原子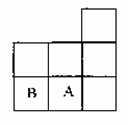 的最外层均达到8个电子的稳定结构。下列说法不正确的是( )
的最外层均达到8个电子的稳定结构。下列说法不正确的是( )
A.该化合物在熔融状态下能导电
B.该化合物的结构式是Cl-S-S-Cl
C该化合物形成的晶体是分子晶体
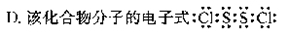
查看答案和解析>>
科目:高中化学 来源: 题型:
空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
 |
(1)步骤④的离子反应方程式为 。
(2)溴微溶于水,步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,它们的相对密度相差较大。分离出液溴的实验室方法为 。
(3)步骤⑥如果在实验室中进行,需用到的玻璃仪器有 。
(4)工业生产不直接蒸馏含溴的海水得到液溴,而要经过“空气吹出、SO2吸收、氯化”,原因是 。
(5)苦卤水还可以用于制取金属镁,用化学方程式表示从苦卤水制取金属镁的反应原理 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com