
| A、25℃时,1L pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA |
| B、标准状况下,1molCF4中含有的电子对数目为4.0NA |
| C、1L 0.5mol?L-1 的H2SO3溶液中含有的H+数目为NA |
| D、1molN2与3molH2混合充分反应后生成NH3分子数小于2.0NA |
| N |
| NA |
| 10-14 |
| 10-13 |
| N |
| NA |


 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
| A、X的原子序数小于Y的原子序数 |
| B、X、Y的核电荷数之差是(m-n) |
| C、Y元素的族序数与X元素的族序数之差是8-(m+n) |
| D、X和Y处于同一周期 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HNO3是氧化剂,NO2是氧化产物 |
| B、还原剂与氧化剂的物质的量比是1:2 |
| C、若2mol Cu完全反应,则反应中共转移了NA个电子 |
| D、氧化产物和还原产物的物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用食醋除去水瓶中的水垢:CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O |
| B、将氯气溶于水制备次氯酸:Cl2+H2O=2H++Cl-+ClO- |
| C、向KHSO4溶液中加入Ba(OH)2溶液至所得溶液的pH=7 Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D、向饱和碳酸氢钙溶液中加入饱和氢氧化钙溶液Ca2++HCO3-+OH-=CaCO3↓++H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
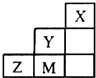 如图为短周期的一部分,推断关于Y、Z、M的说法正确的是( )
如图为短周期的一部分,推断关于Y、Z、M的说法正确的是( )| A、非金属性:Y>Z>M |
| B、阴离子还原性Z2->M- |
| C、原子半径:M>Z>Y |
| D、Y的最高价氧化物的水化物的化学式为HYO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同一元素不可能既有金属性,又有非金属性 |
| B、第2周期主族元素的最高化合价都等于它所在的族序数 |
| C、短周期元素的简单离子,最外层并不都能达到8电子稳定结构 |
| D、同主族元素的原子,最外层电子数相同,因此化学性质也完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯气的水溶液能导电,所以氯气属于电解质 |
| B、稀H2SO4溶液能导电,稀H2SO4是电解质 |
| C、由于NH3?H2O溶于水,而Ca(OH)2微溶于水,所以NH3?H2O是强电解质,Ca(OH)2是弱电解质 |
| D、硫酸钡难溶于水,但硫酸钡属于强电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ①溶解 |
| ②加入NaOH |
| ③加入() |
| ④加入() |
| ⑤过滤 |
| ⑥加入() |
| ⑦() |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com