
下图是某溶液在稀释过程中,溶质的物质的量浓度随溶液体积的变化曲线图,

根据图中数据分析可得出a值等于
A.2 B.3 C.4 D.5
科目:高中化学 来源:2014-2015学年广东省广州市高三上学期期中理综化学试卷(解析版) 题型:选择题
常温下,0.1 mol·L-1的一元酸HA与0.1 mol·L-1的NaOH溶液等体积混合后,所得溶液pH>7,下列说法正确的是
A.混合前一元酸HA的c(H+)=0.1 mol·L-1
B.该混合溶液中:c(Na+)>c(A-)>c(OH-)>c(H+)
C.HA在水溶液中的电离方程式:HA = H+ + A-
D.该混合溶液中:c(A-)+ c(HA)=0.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高二上学期期中化学试卷(解析版) 题型:选择题
25℃、101kPa下,反应2N2O5(g) = 4NO2(g)+O2(g),△H=+56.7 kJ/mol 能自发进行的原因是
A.反应吸热 B.熵增效应大于能量效应
C.熵减小 D.反应放热
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:选择题
取含有 0.02 mol 的硫酸溶液,先投入 0.24 g 镁粉,再滴入NaOH 溶液,当使溶液中的镁离子全部转化为沉淀时, 需要NaOH的物质的量为
A.0.02 mol B.0.03 mol C.0.04 mol D.0.01 mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:选择题
某工厂排出的废液中含有Ba2+、Ag+、Cu2+,用①Na2CO3溶液,②NaOH溶液,
③盐酸三种试剂将它们逐一沉淀并加以分离,加入试剂的正确顺序是
A.②③① B.③②① C.①②③ D.③①②
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:选择题
 是重要的工业原料,铀浓缩一直为国际社会关注。下列有关
是重要的工业原料,铀浓缩一直为国际社会关注。下列有关 的说法正确的是
的说法正确的是
A. 原子核中含有92个中子
原子核中含有92个中子
B. 原子核外有143个电子
原子核外有143个电子
C. 与
与 互为同位素
互为同位素
D. 与
与 为同一核素
为同一核素
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高二上学期期中化学试卷(解析版) 题型:实验题
(12分)用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4-(aq)+5H2C2O4(aq)+6H+(aq)=2Mn2+(aq)+10CO2(g)+8H2O(l) ΔH<0
一实验小组欲通过测定单位时间内生成CO2的体积,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化,所用注射器的容积充裕):
实验序号 | A溶液 | B溶液 |
① | 20 mL 0.1 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |
② | 20 mL 0.2 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |
(1)该实验探究的是 因素对化学反应速率的影响,如果实验完成时草酸与KMnO4均有剩余,则相同时间内针筒中所得CO2体积大小关系是: < (填实验序号)研究发现反应速率总是如图所示发生变化,则t1~t2时间内速率变快的主要原因可能是:①产物Mn2+是反应的催化剂,② 。
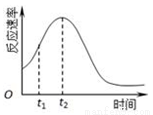
(3)若实验①在4 min末收集了4.48 mL CO2(标准状况),则4 min末c(MnO4-)= mol·L-1(假设溶液混合后体积为50 mL),此4 min内的平均速率为v(H2C2O4)= 。
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可以通过测定 来比较化学反应速率。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高二上学期期中化学试卷(解析版) 题型:选择题
在一定条件下发生反应:2A(g)+2B(g)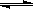 xC(g)+2D(g),在2L密闭容器中,把4molA和2molB混合,2min后达到平衡时生成1.6molC,又测得反应速率V(D)=0.2mol·L-1·min-1,下列说法正确的是
xC(g)+2D(g),在2L密闭容器中,把4molA和2molB混合,2min后达到平衡时生成1.6molC,又测得反应速率V(D)=0.2mol·L-1·min-1,下列说法正确的是
A.A和B的转化率均是20%
B.x = 4
C.平衡时A的物质的量为2.8mol
D.平衡时气体压强比原来减小
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市宝坻区四校高二11月联考化学试卷(解析版) 题型:填空题
(7分)化学反应2A(g) B(g)+D(g)在四种不同条件下进行,B、D的起始浓度为0。反应物A的浓度(mol·L-1)随时间(min)的变化情况如下表:
实验序号 | 温度 | 0 min | 10 min | 20 min | 30min | 40min | 50 min | 60min |
1 | 800℃ | 1.0 | 0.8 | 0.67 | 0.57 | 0.5 | 0.5 | 0.5 |
2 | 800℃ | c2 | 0.6 | 0.5 | 0.5 | 0.5 | 0.5 | 0.5 |
3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.6 | 0.6 | 0.6 |
4 | 820℃ | 1.0 | 0.4 | 0.25 | 02 | 0.2 | 02 | 02 |
根据上述数据,完成下列填空:
(1)在实验1中,反应在10min至20min时间内v(A)的平均速率为 mol·L-1·min-l
(2)在实验2中A的初始浓度为 mol·L-1,由实验2的数据,可推测实验2中还隐含的条件是 。
(3)设实验3的反应速率为v3,实验1的反应速率为vl,则v3 (填“>”、“<”或“=”) vl 。且c3 (填“>”、“<”或“=”)1.0 mol·L-1。
(4)比较实验4和实验1,可推测该反应是 (填“吸热”或“放热”)反应,
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com