
【题目】为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
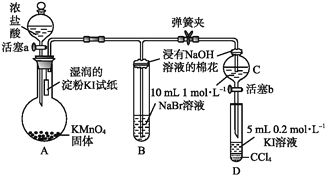
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,其化学方程式是________。
(2)验证氯气的氧化性强于碘的实验现象是________。
(3)B中溶液发生反应的离子方程式是________。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是________。
(5)过程Ⅲ实验的目的是________。
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下________,得电子能力逐渐减弱。
【答案】 16HCl(浓)+2KMnO4===2MnCl2+2KCl+5Cl2↑+8H2O 湿润的淀粉KI试纸变蓝 Cl2+2Br===Br2+2Cl 打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡。静置后CCl4层溶液变为紫红色 确认C的黄色溶液中无Cl2,排除Cl2对溴置换KI溶液中碘的实验的干扰 原子半径逐渐增大
【解析】(1)A中产生黄绿色气体是氯气,反应的化学方程式是16HCl(浓)+2KMnO4=2MnCl2+2KCl+5Cl2↑+8H2O。(2)氯气具有氧化性,能把碘化钾氧化生成单质碘,碘遇淀粉显蓝色,所以验证氯气的氧化性强于碘的实验现象是湿润的淀粉KI试纸变蓝。(3)氯元素的非金属性强于溴元素的非金属性,所以氯气能和溴化钠反应生成单质溴,反应的离子方程式是Cl2+2Br-=Br2+2Cl-。(4)由于C中有单质溴生成,所以要验证溴的氧化性强于碘,过程Ⅳ的操作和现象分别是先打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡。静置后CCl4层溶液变为紫红色。(5)由于氯气也能氧化碘化钾,干扰单质溴和碘化钾的反应,所以过程Ⅲ实验的目的是确认C的黄色溶液中无Cl2,排除Cl2对溴置换碘实验的干扰。(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下原子半径逐渐增大,得电子能力逐渐减弱。


 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
【题目】如图所示,分别向密闭容器内可移动活塞的两边充入空气,H2和O2的混合气体,在标准状态下,若将H2、O2的混合气体点燃引爆。活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来H2、O2的体积之比可能为

A.2∶7 B.5∶4 C.2∶1 D.7∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,利用培养皿探究SO2的性质,实验时向Na2SO3固体上滴几滴浓硫酸,立即用另一表面扣在上面。表中对实验现象的描述或解释不正确的是

选项 | 实验现象 | 解释 |
A | BaCl2溶液变浑浊 | SO2与BaCl2溶液反应产生了BaSO3沉淀 |
B | Na2S溶液变浑浊 | SO2与Na2S溶液反应产生了S单质 |
C | 酸性KMnO4溶液褪色 | SO2具有还原性 |
D | 品红溶液褪色 | SO2具有漂白性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制取Na2S2O3·5H2O的装置图(略去部分夹持仪器)。
已知:Na2SO3 +S![]() Na2S2O3
Na2S2O3
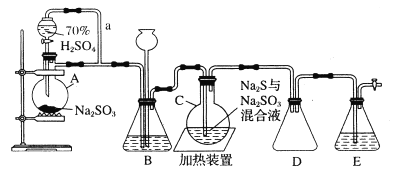
按要求回答下列问题:
(1)仪器A的名称是___________________。
(2)分液漏斗中用70%较浓硫酸的理由是___________________。
(3)装置C中生成S的离子反应方程式是___________________。
(4)E是SO2的尾气处理装置,则装置D的作用是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识完成下面题目:
(1)甲烷(CH4)的摩尔质量为;
(2)8gCH4中约含有个分子,在标准状况下所占的体积约为L;
(3)所含原子数相等的甲烷和氨气(NH3)的质量比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是( )
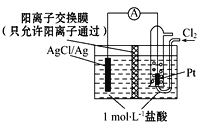
A. 正极反应为AgCl+e-=Ag + Cl-
B. 放电时,交换膜右侧溶液中有大量白色沉淀生成
C. 若用NaCl溶液代替盐酸,则电池总反应随之改变
D. 当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于焰色反应的说法正确的是
A.焰色反应一定属于化学变化
B.观察K2SO4的焰色应透过蓝色的钴玻璃
C.可以用焰色反应鉴别Na与NaCl
D.NaCl与KCl在灼烧时火焰颜色相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
A. NH3、O2、NO、H2O(g)同时存在时,则反应达到化学平衡状态
B. 单位时间内生成x mol NO,同时消耗x mol NH3时,说明反应达到化学平衡状态
C. 达到化学平衡状态时,若增大容器体积,则正反应速率减小,逆反应速率增大
D. 化学反应速率关系是3v正(NH3)=2v正(H2O)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com