
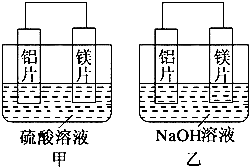
分析 (1)在酸性介质中镁比铝活泼,所以甲中镁易失电子作负极、Al作正极,负极上镁发生氧化反应、正极上氢离子发生还原反应;
(2)在碱性介质中铝比镁活泼,所以乙池中铝易失电子作负极、镁作正极,负极上铝失电子发生氧化反应;
(3)可以通过测电流的方向来判断原电池的正负极.
解答 解:(1)镁易失电子作负极、Al作正极,负极上镁发生氧化反应、正极上氢离子发生还原反应,原电池中阴离子向负极移动,所以硫酸根离子流向镁片,正极的电极反应式为:2H++2e-=H2↑,故答案为:镁片;2H++2e-=H2↑;
(2)在碱性介质中铝比镁活泼,所以乙池中铝易失电子作负极、镁作正极,负极上铝失电子发生氧化反应,总的电极反应式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,氧化剂是水,还原剂是铝,而1mol的水电离产生1mol的氢离子,1mol的氢离子得到1mol的电子,而1mol的转移3mol的电子,所以氧化剂和还原剂的物质的量之比为3:1,故答案为:铝片,2Al+2OH-+2H2O=2AlO2-+3H2↑,3:1;
(3)上述实验说明,“直接利用金属活动性顺序表判断电池中的正负极”并不考可靠,最好是接一个电流计,通过观察电流方向判断原电池的正负极,
故答案为:不可靠;在两电极之间连上一个电流计测电流方向,判断原电池的正负极.
点评 本题考查了探究原电池原理,明确原电池中各个电极上发生的反应是解本题关键,注意不能根据金属的活动性强弱判断正负极,要根据失电子难易程度确定负极,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 1 mol C5H12分子中,含17×6.02×1023个共用电子对 | |
| B. | 10 mL 18.4 mol•L-1的浓硫酸与90 mL蒸馏水混合,所得溶液中c(H+)=3.68 mol•L-1 | |
| C. | 25℃时,在pH=4的HCl溶液与pH=10的Na2CO3溶液中,水电离出的c(H+)前者大于后者 | |
| D. | 25℃时,在25 mL 0.1 mol•L-1NaOH溶液中,滴入0.1 mol•L-1的CH3COOH溶液至混合溶液pH=7时,则滴加CH3COOH溶液的体积大于25 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①和② | B. | ①和③ | C. | ②和③ | D. | 只有③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ⑥ | ② | |||||
| 3 | ③ | ④ | ⑤ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
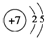 ,⑩的元素名称:溴
,⑩的元素名称:溴 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
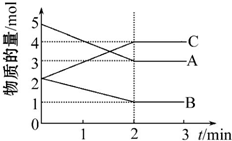
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从NH4HCO3中闻到了刺激性气味 | B. | NaCl颗粒被粉碎 | ||
| C. | I2升华 | D. | NaOH溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将少量金属钠放入冷水中:Na+2H2O=Na++2OH-+H2↑ | |
| B. | 盛放烧碱溶液不用玻璃塞的原因:SiO2+2OH-=SiO32-+H2O | |
| C. | 向磷酸二氢铵溶液中加入足量的氢氧化钠溶液:NH4++OH-=NH3•H2O | |
| D. | 浓硝酸长期放置:4HNO3=4NO↑+3O2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最外层有1个电子的元素一定是金属元素 | |
| B. | 除0族元素外,第三周期元素的原子半径不一定比第二周期元素的原子半径大 | |
| C. | 同主族元素从上到下,元素原子得电子能力逐渐减弱,氢化物的稳定性逐渐增强 | |
| D. | 主族元素的原子,最外层电子数少的一定比最外层电子数多的失电子能力强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (Ⅰ)用 ① | B. | (Ⅱ)用 ② | C. | (Ⅲ)用 ③ | D. | (Ⅳ)用 ④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com