
【题目】下图表示细胞内某些有机物的元素组成和功能关系,其中A、B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ是生物大分子, X、Y、Z、P分别为构成生物大分子的基本单位,请回答下列问题:
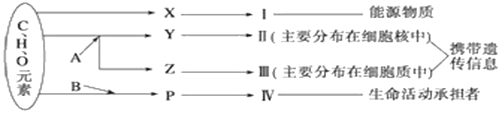
(1)Ⅰ在小麦种子中主要是指______,其基本单位X是______。
(2)A代表的元素是____,Ⅱ是____,Ⅲ是RNA,Z是_____。
(3)Ⅳ一定含有的元素有______。P的结构通式是______,图中由P形成Ⅳ的反应方式称为____,Ⅳ的特定功能的发挥与其_____结构有关。若P的平均相对分子质量r,由多个P形成m条肽链,经盘曲折叠形成了相对分子质量为e的Ⅳ,则Ⅳ分子中肽键的数目是__________。
【答案】淀粉葡萄糖N、PDNA核糖核苷酸CHON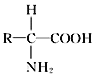 脱水缩合空间结构e-rm/r-18
脱水缩合空间结构e-rm/r-18
【解析】
根据题意和图示分析可知:A代表N、P元素,B代表N元素、X为葡萄糖、Y为脱氧核苷酸、Z为核糖核苷酸、P为氨基酸;Ⅰ表示糖类、Ⅱ表示DNA、Ⅲ表示RNA、Ⅳ表示蛋白质。
(1)Ⅰ代表的是多糖,在小麦种子中主要指的是淀粉,淀粉是由葡萄糖脱水缩合而成,故基本单位为葡萄糖。
(2)组成核酸的组成元素是C、H、O、N、P,故A代表的元素是N、P,Ⅱ携带遗传信息主要分布在细胞核则为DNA,RNA的基本单位是核糖核苷酸。
(3)Ⅳ是生命活动的承担着即蛋白质,蛋白质的组成元素中一定含有C、H、O、N,其基本单位是氨基酸,氨基酸通过脱水缩合的方式形成多肽,折叠形成具有空间结构的蛋白质,设总共有氨基酸x个,则氨基酸的总相对分子质量为:rx,由脱水缩合形成m条肽链可知,失去的水分子数为x-m,则失去的水分子的相对分子量为18(x-m),蛋白质的相对分子质量=总的氨基酸总相对分子量-失去的水分子相对分子质量,即:e=rx-18(x-m) 得:x=(e-18m)/(r-18),又由于:失去的水分子数=肽键数 得:x-m=(e-rm)/(r-18)。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】大气细颗粒物吸附的水分中NO2与SO2的化学反应是当前雾霾期间硫酸盐的主要生成路径。某实验小组对雾霾的成分进行了验证,并测定空气中SO2的含量及探究H2SO3的部分性质。
回答下列问题:
(1)硫酸铵是某地PM2.5雾霾的主要成分,收集一定量的雾霾固体进行验证。
取一定量的雾霾固体于试管中,加入适量的水溶解,把溶液分成两份盛于试管中:
操作步骤 | 实验现象 | 结论 |
①向其中一份_______ | 有白色沉淀生成 | 证明雾霾固体中含有SO42- |
②向另一份中_____,用镊子夹持湿润的红色石蕊试纸靠近试管口 | ③试管中有气泡产生,___________________ | 证明雾霾固体中含有NH4+。综合上面实验,初步说明雾霾固休颗粒中含有(NH4)2SO4 |
(2)用如图所示简易装置测定空气中SO2的含量。
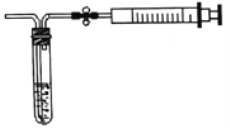
①测定原理:SO2通入碘的淀粉溶液中,使溶液由蓝色变为无色,反应的化学方程式为______。
②测定方法:在某监测点,量取5.0mL5.0×10-4mol/L的碘溶液,注入图中的试管中,加2-3滴淀粉指示剂,此时溶液呈蓝色,按图中装置连接好仪器,利用止水夹控制,进行抽气,取下注射器排气,重复操作直到溶液的蓝色全部褪尽为止,共抽取空气8000.0mL,则测得该监测点空气中SO2的含量为_____mg/L。
(3)探究H2SO3的部分性质。
选用下面的装置和药品探究H2SO3与HClO的酸性强弱
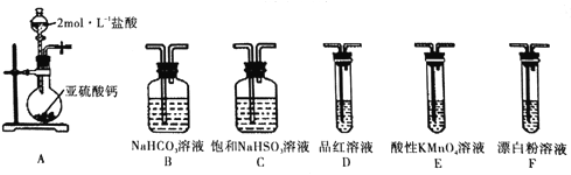
①甲同学认为按照A→C→F→尾气处理的顺序连接装置,可以证明H2SO3与HClO的酸性强弱,乙同学认为该方案不合理,其理由是_________________。
②丙同学采用间接法证明,实验方案为:按照A→C____(其字母) →尾气处理顺序连接装置,其中装置C的作用是___________;证明H2SO3的酸性强于HClO的酸性的实验现象是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图表示细胞四种有机物的组成。依据生物功能,分析回答下列问题:
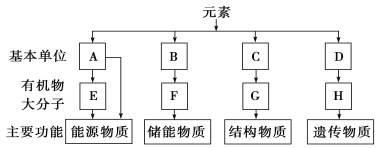
(1)A是指________;E在动物细胞内是指________,在植物细胞内主要是指________。
(2)F是指________;它是由B(脂肪酸和甘油)形成的,除此之外,脂质还包括________ 和________。
(3)C是指________,通式是________;C形成G过程的反应叫________。
(4)D是指________,H是指________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温条件下,欲使CH3COONa的稀溶液中c(CH3COO-)/c(Na+)比值增大,可在溶液中加入少量下列物质中的( )
①固体NaOH ②固体KOH ③固体NaHSO4 ④固体CH3COONa ⑤冰醋酸
A. 只有②⑤ B. 只有①②⑤
C. 只有①② D. 只有②④⑤
【答案】D
【解析】加入固体NaOH,溶液中c(Na+)明显增大,虽然氢氧根离子会抑制醋酸根离子的水解,但是c(CH3COO-)的增大一定不明显,所以c(CH3COO-)/c(Na+)比值减小,①错误。加入固体KOH,氢氧根离子会抑制CH3COONa的水解,c(CH3COO-)增大,c(CH3COO-)/c(Na+)比值增大,②正确。加入固体NaHSO4,溶液中c(Na+)明显增大,同时电离出的氢离子会促进CH3COONa的水解,c(CH3COO-)减小,c(CH3COO-)/c(Na+)比值减小,③错误。加入固体CH3COONa,增大了溶液中的CH3COONa浓度,浓度越大CH3COONa的水解成都越小,所以c(CH3COO-)/c(Na+)比值越大,④正确。加入冰醋酸,醋酸电离会增大c(CH3COO-),c(CH3COO-)/c(Na+)比值增大,⑤正确。所以正确的是②④⑤,选项D正确。
【题型】单选题
【结束】
16
【题目】40℃时,在氨—水体系中不断通入CO2,各种离子的变化趋势如下图所示。下列说法不正确的是( )
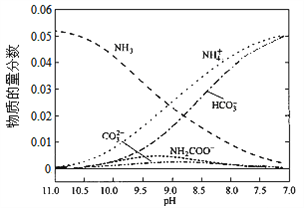
A. 在pH=9.0时,c(NH4+)>c(HCO3-)>c(NH2COO-)>c(CO32-)
B. 不同pH的溶液中存在关系:c(NH4+)+c(H+)=2c(CO32-)+c(HCO3-)+c(NH2COO-)+c(OH-)
C. 在溶液中pH不断降低的过程中,有含NH2COOˉ的中间产物生成
D. 随着CO2的通入,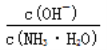 不断增大
不断增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学-物质结构与性质】许多过渡元素(如锰、钒、铬、铁、铜等)的化合物对化学反应具有良好的催化性。回答下列问题:
(1)基态铬原子的价层电子排布式为_________;Mn2+的稳定性强于Mn3+,其原因是_______。
(2)已知常温下,H2CrO4的K1=4.1、K2=1×10-5,从结构的角度上看,K2<<K1的原因是_________。已知Cr2(SO4)3的熔点为100℃、沸点为330℃,则Cr2(SO4)3晶体中微粒间的相互作用力是__________。
(3)SO2与氧气在V2O5催化作用下反应可转化为SO3,则转化过程中_____(填字母)没有发生变化。
a.中心原子轨道杂化类型 b.键角 c.分子的极性
(4)+5价钒能形成多种含氧酸根盐,其中某种钠盐的酸根离子是一种具有无限链状结构的离子(见下图),则该酸根离子的化学式为__________。
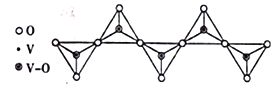
(5)CuSO4溶液中Cu2+是以[Cu(H2O)4]2+形式存在的,向CuSO4溶液中加入过量氨水后会得到[Cu(NH3)4]2+,则上述两种配离子中稳定性较强的是_________,N、O、S、Cu四种元素的第一电离能由大到小的顺序为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下, ![]() 溶液发生催化分解。不同时刻测得生成
溶液发生催化分解。不同时刻测得生成![]() 的体积(已折算为标准状况)如下表。
的体积(已折算为标准状况)如下表。
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
A. ![]() 的平均反应速率:
的平均反应速率: ![]()
B. ![]() 的平均反应速率:
的平均反应速率: ![]()
C. 反应到![]() 时,
时, ![]()
D. 反应到![]() 时,
时, ![]() 分解了50%
分解了50%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com