
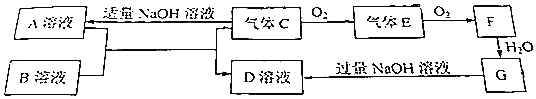
���� E��F����Է����������16����ת����ϵ��֪EΪSO2��FΪSO3����GΪH2SO4��DΪNa2SO4��CΪH2S����AΪNaHS��BΪNaHSO4���Դ˽����⣮
��� �⣺��1�������Ϸ�����֪BΪNaHSO4��FΪSO3��DΪNa2SO4���ʴ�Ϊ��NaHSO4��SO3��Na2SO4��
��2��AΪNaHS��BΪNaHSO4������Ϸ�Ӧ�����ӷ���ʽΪHS-+H+=H2S��H2S���л�ԭ�ԣ��ɱ���ˮ��������Ӧ�����ӷ���ʽΪH2S+Br2=S��+2H++Br-������������巢��������ԭ��Ӧ����HBr�����ᣬ���ӷ���ʽΪSO2+Br2+2H2O=4H++2Br-+SO42-��
�ʴ�Ϊ��HS-+H+=H2S��H2S+Br2=S��+2H++Br-��SO2+Br2+2H2O=4H++2Br-+SO42-��
��3��GΪH2SO4���ڼ��������¿���Cu��Ӧ���ɶ���������ʽΪ2H2SO4+Cu$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O���ʴ�Ϊ��2H2SO4+Cu$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
���� ���⿼��������ƶϣ�Ϊ�߿��������ͣ���Ŀ�ѶȽϴ�ע��������ʵ�������Ϊ�ƶϵ�ͻ�ƿڣ����ʱע����ջ�ѧ����ʽ����д���������ʵ����ʣ��жϷ�Ӧԭ���ǹؼ�����Ŀ����������ѧ���ķ���������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al$��_{��}^{O_{2}}$Al2O3 $\stackrel{HNO_{3}}{��}$Al��NO3��3$��_{��}^{���ɡ�����}$Al2O3 | |
| B�� | Cu$��_{��}^{O_{2}}$CuO$\stackrel{ϡ����}{��}$CuSO4��Һ$\stackrel{�������ᾧ}{��}$CuSO4•5H2O | |
| C�� | Fe$\stackrel{Cl_{2}}{��}$FeCl3$\stackrel{������ˮ}{��}$Fe��OH��3$\stackrel{����}{��}$Fe2O3 | |
| D�� | FeSO4��Һ$\stackrel{H_{2}S}{��}$FeS$\stackrel{��������}{��}$FeS |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
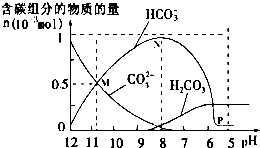 25��ʱ��10mL0.10mol•L-1Na2CO3��Һ����μ���0.10mol•L-1HCl��Һ20mL����Һ�в��ֺ�̼�������ʵ�������ҺpH�ı仯��ͼ��ʾ������˵����ȷ���ǣ�������
25��ʱ��10mL0.10mol•L-1Na2CO3��Һ����μ���0.10mol•L-1HCl��Һ20mL����Һ�в��ֺ�̼�������ʵ�������ҺpH�ı仯��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | pH=12����Һ�У�c��Na+��=c��CO32-��+c��HCO3-��+c��H2CO3�� | |
| B�� | pH=7����Һ�У�c��Na+��=2c��CO32-��+c��HCO3-��+c��Cl-�� | |
| C�� | pH=8����Һ�У�c��Na+����c��HCO3-����c��Cl-����c��OH-�� | |
| D�� | ��M�㣺c��Na+����c��CO32-��=c��HCO3-����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��CH3COOH�ܽ�CaCO3��CaCO3+2H+�TCa2++H2O+CO2�� | |
| B�� | Fe2��SO4��3��Ba��OH��2��Һ��ϣ�2Fe3++3SO42-+3Ba2++6OH-�T2Fe��OH��3��+3BaSO4�� | |
| C�� | ���Ṥ��β���е�SO2�ù����İ�ˮ���գ�2NH3•H2O+SO2�T2NH4++SO32-+H2O | |
| D�� | Cu����ŨHNO3��Cu+4H++2NO3-�TCu2++2NO��+4H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | �ױ� | C�� | �ұ� | D�� | ������ϩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
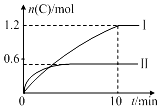 ��2L�ĺ����ܱ������г���A��g����B��g����������Ӧ��A��g��+B��g��?2C��g��+D��s����H=a kJ•mol-1ʵ�����ݺͽ���ֱ������ͼ��ʾ������˵����ȷ���ǣ�������
��2L�ĺ����ܱ������г���A��g����B��g����������Ӧ��A��g��+B��g��?2C��g��+D��s����H=a kJ•mol-1ʵ�����ݺͽ���ֱ������ͼ��ʾ������˵����ȷ���ǣ�������| ʵ����� | �¶� | ��ʼ���ʵ��� | �����仯 | |
| A | B | |||
| �� | 600�� | 1 mol | 3 mol | 96 kJ |
| �� | 800�� | 0.5 mol | 1.5 mol | -- |
| A�� | a=160 | |
| B�� | 600��ʱ���÷�Ӧ��ƽ�ⳣ����0.45 | |
| C�� | ʵ����У�10 min��ƽ������v��B��=0.06 mol•L-1•min-1 | |
| D�� | ��ʵ����ƽ����ϵ���ٳ���0.5 mol A��1.5 mol B��A��ת���ʲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 34gH2O2�к��е���������Ϊ1NA | |
| B�� | 4.6g�Ҵ��к��е�C-H���ĸ���Ϊ0.6NA | |
| C�� | ��״���£�VLˮ���е���ԭ�Ӹ���ԼΪ$\frac{V}{22.4}$ | |
| D�� | 1molFe2+��������H2O2��Һ��Ӧ��ת��NA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | ��SiO2 | ��C | Na2O�� | ��K2O | Al2O3 | ��Fe2O3 |
| ����������/% | ��59.20 | ��38.80 | ��0.25 | ��0.50 | ��0.64 | 0.16 |

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com