
 如图为Zn-Cu原电池的示意图,请回答:
如图为Zn-Cu原电池的示意图,请回答:

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 有原子序数依次增大的4种短周期元素X、Y、Z、W,已知:
有原子序数依次增大的4种短周期元素X、Y、Z、W,已知:查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 编号 |
实验目的 | 温度/℃ | 催化剂 质量/g |
反应物初始浓度 /10-3mol?L-1 | |
| H2 | I2 | ||||
| Ⅰ | 为以下两个实验作参照 | 457 | 0 | 7 | 9 |
| Ⅱ | 420 | 0 | 7 | 9 | |
| Ⅲ | 探究催化剂对该反应速率的影响 | 10 | 7 | 9 | |
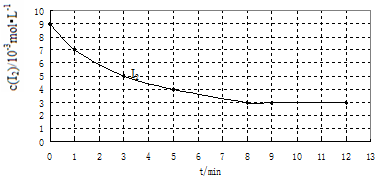
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 图中A为淡黄色固体,B、C为液体,D为气体,E、F为白色沉淀.
图中A为淡黄色固体,B、C为液体,D为气体,E、F为白色沉淀.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Na+、NO3-、CO32- |
| B、Mg2+、C1-、OH-、SO42- |
| C、Ca2+、Na+、Fe3+、NO3- |
| D、K+、Cl-、HCO3-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜片插到硝酸银溶液中:Cu+2Ag+=Cu2++2Ag |
| B、铜与稀硫酸反应:Cu+2H+=Cu2++H2↑ |
| C、碳酸氢钠溶液与稀盐酸混合:HCO3-+H+=CO2↑+H2O |
| D、氢氧化钡溶液与稀硫酸混合:Ba2++H++OH-+SO42-=BaSO4↓+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com