
在反应中,元素X的原子将电子转移给元素Y的原子,则下列说法正确的是( )
①元素X被氧化 ②元素Y被氧化 ③元素X发生还原反应 ④元素Y发生还原反应
A.①② B.③④ C.②③ D.①④
科目:高中化学 来源: 题型:
黄铜矿(CuFeS2)是炼钢和炼铜的主要原料.在高温下灼烧生成二氰化二铁和氰化亚铜。三氧化二铁和氧化亚铜都是红色粉末.常用作颜料。某学校化学兴趣小组通过实验米探究一红色粉末是Fe2O3、Cu2O或两者的混合物。探究过程如下:
【查阅资料】Cu2是一种碱性氧化物.溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO。
【提出假设】
假设1:红色粉末是Fe2O3。
假设2:红色粉末是Cu2O。
假设3:红色粉末是Fe2O3和Cu2O的混合物。
【设计探究实验】
取少量粉末放入足量稀硫酸中.在所得溶液中再滴加KSCN试剂。
(1)若假设1成立,则实验现象是 。
(2)滴加KSCN试剂后溶液不变红色.某同学认为原同体粉末中一定不含二氰化二铁。你认为这种说法合
理吗? 。简述你的理由(不需写出反应的化学方程式): 。
(3)若同体粉末完伞溶解尢同体存在.滴加KSCN试剂时溶液不变红色.则证明原同体粉末是 ,写出发生的氧化还原反应的离子方程式: 。
【探究延伸】
(4)绎实验分析.确定红色粉末为Fe2O3和Cu2O的混合物。实验小组欲利用该红色粉末制取较纯净的胆矾(CuSO4·5H2O)。纤杏阅资料得知.在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
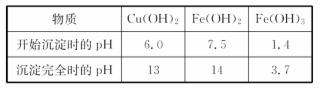
实验小组设汁如下实验方案:
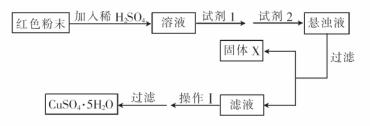
①试剂1为 .试剂2为 . (填字母)
A.氯水 B.H2O2 C.NaOH
②同体X的化学式为 。
③操作II为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列能说明氯元素原子得电子能力比硫强的是( )
①HCl的溶解度比H2S大 ②HCl的酸性比H2S强③HCl的稳定性比H2S强 ④HCl的还原性比H2S强⑤HClO的酸性比H2SO4强 ⑥Cl2能与H2S反应生成S ⑦Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑧还原性:Cl- <S2-
A.③④⑤⑧ B.③⑥⑦ C.③⑥⑦⑧ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
乙酰苯胺作为一种常用药,具有解热镇痛的效果。实验室制备乙酰苯胺时,可以用苯胺与乙酸酐或与冰醋酸加热来制取,苯胺与乙酸酐的反应速率远大于与冰醋酸反应的速率,已知苯胺微溶于冷水;纯乙酰苯胺是无色片状晶体,熔点114℃,不溶于冷水,可溶于热水;乙酸酐遇水缓慢反应生成乙酸;现选用苯胺与乙酸酐为原料制取和提纯乙酰苯胺,该放热反应的原理:
 |
实验步骤
① 取5.0 mL苯胺(密度1.04 g/mL),倒入100 mL锥形瓶中,加入20 mL水,在旋摇下分批加入6.0 mL乙酸酐(密度1.08 g/mL),搅拌均匀。若有结块现象产生,用玻璃棒将块状物研碎,再充分搅拌;
② 反应完全后,及时把反应混合物转移到烧杯中,冷却后,抽滤,洗涤,得粗乙酰苯胺固体;
③ 将粗产品转移至150 mL烧杯中,加入适量水配制成80℃的饱和溶液,再加入过量20%的水。稍冷后,加半匙活性炭,搅拌下将溶液煮沸3~5 min,过滤Ⅰ,用少量沸水淋洗烧杯和漏斗中的固体,合并滤液,冷却结晶,过滤Ⅱ、洗涤、晾干得乙酰苯胺纯品。
(1)步骤①研碎块状产物的用意在于 ;反应温度过高会导致苯胺挥发,下列可以控制反应温度,防止反应温度升高过快的操作有 ;
A.反应快结束时的充分搅拌 B.旋摇下分批加入6.0 mL乙酸酐
C.玻璃棒将块状物研碎 D.加20ml水
(2)步骤②洗涤粗产品时,选用的溶剂是 ;
A.热水 B.冷水 C.1:3的乙醇溶液 D.滤液
(3)步骤③两次用到过滤,其中过滤Ⅰ选择 (过滤、趁热过滤或抽滤),过滤Ⅰ操作是为了除去 ;配制热溶液时,加入过量溶剂的作用是
(选出正确选项);
A.防止后续过程中,溶剂损失可能产生的产物析出
B.防止后续过程中,温度降低可能产生的产物析出
C.除去活性炭未吸附完全的有色杂质
(4)步骤③冷却滤液时可选择 ;
A.冰水浴冷却 B.搅拌下水浴冷却
C.室温下自然冷却 D.投入少量碎冰后静置
(5)步骤③中以下哪些操作不能提高产率 ;
① 配制成饱和溶液后,加入过量20%的溶剂;② 趁热过滤近沸溶液;③ 过滤Ⅰ时用少量沸水淋洗烧杯和漏斗中的固体,合并滤液;④ 加活性炭吸附;⑤ 过滤Ⅱ时的洗涤选用热水代替冷水洗涤固体。
A.①④⑤ B.①④ C.④⑤ D.②④⑤
(6)步骤③最后测得纯乙酰苯胺固体6.75g,已知苯胺、乙酸酐和乙酰苯胺的摩尔质量分别为93g/mol、102g/mol、135g/mol。该实验的产率为 (保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质,按化合物、单质、混合物顺序排列的是( )
A 烧碱、液态氧、碘酒 B 生石灰、白磷、熟石灰
C 干冰、铁、氯化氢 D 空气、氮气、胆矾
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)绿色食品是指( )
A.绿颜色的营养食品 B.有叶绿素的营养食品
C.附加值高的营养食品 D.安全、无公害的营养食品
(2)下列垃圾中,不适合用卫生填埋、焚烧、堆肥等处理方法处理的是( )
A.腐败食品 B.电池 C.卫生纸 D.纯棉纺织品
(3)葡萄糖能发生银镜反应说明其结构中含有 基。
(4)维生素C可以与酸性高锰酸钾溶液反应,高锰酸钾中的锰元素生成正二价锰离子,那么维生素C发生了 (填“氧化”或“还原” )反应
(5)油脂被摄入人体后,在酶的作用下水解为高级脂肪酸和 (写名称),进而被氧化生成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料。
(6)氨基酸是组成蛋白质的基本结构单元,人体中共有二十多种氨基酸,其中人体自身
___ (填“能”或“不能”)合成的氨基酸称为人体必需氨基酸。
(7)淀粉在淀粉酶的作用下最终水解为葡萄糖(C6H12O6),部分葡萄糖在体内被氧化生成二氧化碳和水。写出葡萄糖在体内被氧化的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
氯化铁是一种重要的化工原料,无水氯化铁遇潮湿空气极易吸水生成
FeCl3.nH2O。
(1)实验室用如下装置(部分加热、夹持等装置已略去)制备无水氯化铁固体。
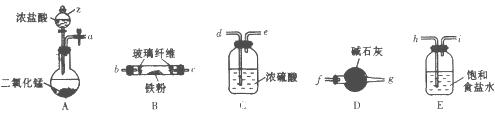
①装置A中仪器z的名称是___________。
②简述检验装置A气密性的操作:______________________。
③按气流方向连接各仪器接口,顺序为a→_________ →__________ →_________ →__________→b→c→_________→__________,装置D的作用是______________________。
(2)工业上制备无水的一种工艺流程如下:
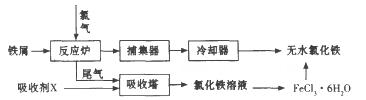
①吸收塔中发生反应的离子方程式为_________________________________________。
②简述由FeCl3.6H2O晶体得到无水氯化铁的操作:________________________________。
③用碘量法测定所得无水氯化铁的质量分数:称取m克无水氯化铁样品,溶于稀盐酸,再转移到100 mL容量瓶中,用蒸馏水定容;取出10 mL,加入稍过量的KI溶液,充分反应后,滴入指示剂_________(填试剂名称),用c mol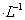 的Na2S2O3溶液进行滴定,终点时消耗V mLNa2S2O3溶液(已知:
的Na2S2O3溶液进行滴定,终点时消耗V mLNa2S2O3溶液(已知: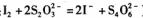 )。则样品中氯化铁的质量分数为____________。
)。则样品中氯化铁的质量分数为____________。
(3)若已知:

请写出Fe3+发生水解反应的热化学方程式________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于Na2CO3和NaHCO3比较中,下列说法不正确的是
A.NaHCO3固体受热容易分解,而Na2CO3固体受热不容易分解
B.等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,前者消耗盐酸的物质的量比后者多
C.等物质的量浓度的Na2CO3和NaHCO3溶液分别滴加2滴酚酞试液,前者颜色比后者深
D.Na2CO3溶液和NaHCO3溶液分别与Ba(OH)2溶液反应的离子方程式相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com