
【题目】铜的相关化合物在生产生活中具有重要的作用。
回答下列问题:
(1)铜元素在周期表中的位置是____,基态铜原子中,核外电子占据最高能层的符号是___,占据该最高能层的电子数为_________。
(2)在一定条件下,金属相互化合形成的化合物称为金属互化物,如Cu9Al4、Cu6Zn8等。某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于___(填“晶体”或”非晶体”)。
(3)铜能与类卤素[(SCN)2]反应生成Cu(SCN)2,1mol(SCN)2分子中含有σ键的数目为_____。
(SCN)2对应的酸有硫氰酸(H-S-C≡N)、异硫氰酸(H-N=C=S)两种,理论上前者沸点低于后者,其原因是__________。
(4)铜晶体中铜原子的堆积方式为面心立方堆积,每个铜原子周围距离最近的铜原子个数为__。
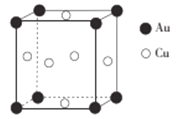
(5)铜与金形成的金属互化物的晶胞结构如图所示,其晶胞边长为anm,该金属互化物的密度为_____________(用含a、NA的代数式表示)g/cm3。
【答案】 第四周期IB族 N 1 晶体 5NA(或5×6.02×1023) 异硫氰酸分子间可形成氢鍵,而硫氰酸不能 12 3.89×1023/(a3NA)
【解析】分析:(1)根据Cu的原子结构示意图和核外电子排布式确定Cu在周期表中的位置、最高能层的符号和最高能层的电子数。
(2)根据晶体和非晶体的本质差异判断,晶体具有自范性、原子在三维空间呈周期性有序排列。
(3)(SCN)2的结构式为N![]() C—S—S—C
C—S—S—C![]() N,单键全为σ键,三键中有1个σ键和2个π键;异硫氰酸分子间形成氢键,沸点较高。
N,单键全为σ键,三键中有1个σ键和2个π键;异硫氰酸分子间形成氢键,沸点较高。
(4)铜原子的堆积方式为面心立方堆积,晶胞中Cu位于8个顶点和6个面心,以顶点Cu原子为研究对象,与之等距离最近的原子处于面心,顶点为8个晶胞共用,面心为2个晶胞共用,则每个铜原子周围距离最近的铜原子个数为![]() =12。
=12。
(5)用“均摊法”确定晶胞中原子个数和化学式,由晶胞边长计算晶胞体积,计算1mol晶体的体积和质量,1mol晶体的质量除以1mol晶体的体积得出晶体的密度。
详解:(1)Cu原子核外有29个电子,Cu原子结构示意图为![]() ,基态Cu原子的核外电子排布式为1s22s22p63s23p63d104s1,Cu在元素周期表中位于第四周期IB族。基态Cu原子中,核外电子占据最高能层是第四能层,第四能层的符号是N。占据该最高能层的电子数为1。
,基态Cu原子的核外电子排布式为1s22s22p63s23p63d104s1,Cu在元素周期表中位于第四周期IB族。基态Cu原子中,核外电子占据最高能层是第四能层,第四能层的符号是N。占据该最高能层的电子数为1。
(2)某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于晶体。
(3)(SCN)2的结构式为N![]() C—S—S—C
C—S—S—C![]() N,单键全为σ键,三键中有1个σ键和2个π键,1个(SCN)2中含5个σ键,1mol(SCN)2分子中含有5molσ键,含σ键的数目为5NA。异硫氰酸分子间形成氢键,硫氰酸分子间不存在氢键,硫氰酸的沸点低于异硫氰酸。
N,单键全为σ键,三键中有1个σ键和2个π键,1个(SCN)2中含5个σ键,1mol(SCN)2分子中含有5molσ键,含σ键的数目为5NA。异硫氰酸分子间形成氢键,硫氰酸分子间不存在氢键,硫氰酸的沸点低于异硫氰酸。
(4)铜晶体中铜原子的堆积方式为面心立方堆积,晶胞中Cu位于8个顶点和6个面心,以顶点Cu原子为研究对象,与之等距离最近的原子处于面心,顶点为8个晶胞共用,面心为2个晶胞共用,则每个铜原子周围距离最近的铜原子个数为![]() =12。
=12。
(5)用“均摊法”,1个晶胞中含Au:8![]() =1个,Cu:6
=1个,Cu:6![]() =3个,金属互化物的化学式为Cu3Au;1个晶胞的体积为(a
=3个,金属互化物的化学式为Cu3Au;1个晶胞的体积为(a![]() 10-7cm)3=a3
10-7cm)3=a3![]() 10-21cm3,1mol晶体的体积为a3
10-21cm3,1mol晶体的体积为a3![]() 10-21cm3
10-21cm3![]() NA=a3
NA=a3![]() NA
NA![]() 10-21cm3,1mol晶体的质量为389g,该金属互化物的密度为389g
10-21cm3,1mol晶体的质量为389g,该金属互化物的密度为389g![]() (a3
(a3![]() NA
NA![]() 10-21cm3)=
10-21cm3)=![]() g/cm3。
g/cm3。


科目:高中化学 来源: 题型:
【题目】在容积为10 L的密闭容器中充入1mol H2和1mol I2,并在一定温度下使其发生反应:H2(g)+I2(g) ![]() 2HI(g)。20min后达到平衡,测得c(HI)=0.04 mol/L。
2HI(g)。20min后达到平衡,测得c(HI)=0.04 mol/L。
(1)反应从开始到平衡时,v(H2)为_______,平衡常数K=__________。
(2)温度不变,达到平衡后向容器中再充入1molHI气体,平衡向________ (填“正向”、“逆向”或“不移动”)移动;再次平衡后,HI的体积分数将________ (填“增大”、“减小”或“不变”)
(3)将(2)所得平衡体系升温,平衡后I2的体积分数为45%,则升温后,H2的转化率将_____(填“增大”、“减小”或“不 变”),该反应的ΔH_____0(填“>”、“ <”或“=”)。
(4)结合(3)请画出2HI(g)![]() H2(g)+I2(g)的平衡常数K随温度变化的趋势图。
H2(g)+I2(g)的平衡常数K随温度变化的趋势图。
 _____
_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)根据元素周期律,碳的非金属性强于硅,请用一个化学反应方程式表示___________________。
(2)若FeSO4和O2的系数比为2∶1,试配平下列方程式:
![]() FeSO4+
FeSO4+![]() K2O2→
K2O2→![]() K2FeO4+
K2FeO4+![]() K2O+
K2O+![]() K2SO4+
K2SO4+![]() O2↑ __________________
O2↑ __________________
(3)各种氮氧化物(NO、NO2)是主要的大气污染物之一,治理氮氧化物(NOx)废气的方法之一是用NaOH溶液进行吸收,现有NO与NO2的混合气体,将其通入50 mL 2 mol/L的NaOH溶液中,恰好完全吸收,测得溶液中含有NO3- 0.02 mol。
①所得溶液中NaNO2的物质的量为________ mol;
②混合气体中V(NO)∶V(NO2)=________。
(4)As2O3俗称砒霜,As2O3是两性偏酸性氧化物,是亚砷酸(H3AsO3)的酸酐,易溶于碱生成亚砷酸盐,写出As2O3与足量氢氧化钠溶液反应的离子方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】上海世博园地区的一座大型钢铁厂搬迁后,附近居民将不再受到该厂产生的棕红色烟的困扰。你估计这一空气污染物是因为含有( )
A.FeO粉尘B.Fe2O3粉尘C.Fe粉尘D.碳粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,H2A是一种易溶于水的二元酸,将NaOH溶液滴入等物质的量浓度的H2A溶液中,溶液中H2A、HA-、A2-的物质的量分数(a)随溶液pH的变化关系如图所示。下列说法错误的是

A. 常温下,H2A![]() HA-+H+的电离平衡常数Ka1=10-3.30
HA-+H+的电离平衡常数Ka1=10-3.30
B. 当c(Na+)=2c(A2-)+c(HA-)时,溶液呈中性
C. pH=6.27时,c(A2-)=c(HA-)>c(H+)>c(OH-)
D. V(NaOH溶液):V(HA溶液)=3:2时,2c(Na+)+c(OH-)=2c(H2A)+c(HA-)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚氯乙烯(PVC)保鲜膜的安全问题引起广泛关注。PVC的安全隐患主要来自于塑料中残留的PVC单体以及不符合国家标准的增塑剂DEHA。工业上用乙烯和氯气为原料经下列各步合成PVC:
![]()
(1)乙是PVC的单体,其结构简式为_____________________;
(2)反应①的化学方程式为______________________________________________________;
(3)写出以下反应类型:反应②_________________;反应③_________________。
(4)邻苯二甲酸辛酯(DOP)是国家标准中允许使用的增塑剂之一,邻苯二甲酸( )是制造DOP的原料,它跟过量的甲醇反应能得到另一种增塑剂DMP(分子式为C10H10O4),DMP属于芳香酯,请写出DMP的结构简式为________________。
)是制造DOP的原料,它跟过量的甲醇反应能得到另一种增塑剂DMP(分子式为C10H10O4),DMP属于芳香酯,请写出DMP的结构简式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由一氧化碳、甲烷和乙烷组成的混合气体8.96L(标准状况),在足量氧气中充分燃烧后,生成气体先通过足量浓硫酸、再通过足量氢氧化钠溶液,测知氢氧化钠溶液增重26.4g,则原混合气体中乙烷的物质的量为
A. 0.1mol B. 0.2mol
C. 大于或等于0.2mo1,小于0.3mol D. 大于0.1mol,小于0.3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原电池的叙述中,正确的是( )
A.原电池的负极上发生还原反应
B.原电池工作时,电子总是由负极经导线流入正极
C.原电池中,正、负极的电极材料一定都是金属单质
D.酸碱中和反应也可以设计成原电池
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com