
【题目】已知2SO2(g)+O2(g)![]() 2SO3(g) △H=-197kJ/mol。在25℃时,向恒容密闭容器中通入2 mol SO2和1 mol O2,达到平衡时放出热量Q1;若25℃时在此恒容密闭容器中只通入1 mol SO2和0.5 mol O2,达到平衡时放出热量Q2。则下列关系正确的是
2SO3(g) △H=-197kJ/mol。在25℃时,向恒容密闭容器中通入2 mol SO2和1 mol O2,达到平衡时放出热量Q1;若25℃时在此恒容密闭容器中只通入1 mol SO2和0.5 mol O2,达到平衡时放出热量Q2。则下列关系正确的是
A. Q2>Q1>197 kJ B. 2Q2<Q1<197 kJ
C. 2Q2=Q1=197 kJ D. 197 kJ> Q1=2Q2
【答案】B
【解析】
2SO2(g)+O2(g)![]() 2SO3(g) △H=-197kJ/mol,表示在上述条件下2mol SO2和1molO2完全反应生成2molSO3气体放出热量为197kJ,再结合可逆反应中反应物不能完全反应解答。
2SO3(g) △H=-197kJ/mol,表示在上述条件下2mol SO2和1molO2完全反应生成2molSO3气体放出热量为197kJ,再结合可逆反应中反应物不能完全反应解答。
反应的热化学方程式为:2SO2(g)+O2(g)![]() 2SO3(g) △H=-197kJ/mol,由热化学方程式可知,在上述条件下反应生成2molSO3气体放热197kJ,加入2mol SO2和1molO2,生成SO3的物质的量小于2mol,所以Q1<197kJ,通入1mol SO2和0.5molO2,如果转化率与加入2mol SO2和1molO2相同,则放热为Q1/2kJ,但此时体系压强比加入2mol SO2和1molO2要小,所以平衡会向左移动,则实际放出的热量小于Q1/2kJ,即2Q2<Q1,综上得:2Q2<Q1<197kJ,答案选B。
2SO3(g) △H=-197kJ/mol,由热化学方程式可知,在上述条件下反应生成2molSO3气体放热197kJ,加入2mol SO2和1molO2,生成SO3的物质的量小于2mol,所以Q1<197kJ,通入1mol SO2和0.5molO2,如果转化率与加入2mol SO2和1molO2相同,则放热为Q1/2kJ,但此时体系压强比加入2mol SO2和1molO2要小,所以平衡会向左移动,则实际放出的热量小于Q1/2kJ,即2Q2<Q1,综上得:2Q2<Q1<197kJ,答案选B。


科目:高中化学 来源: 题型:
【题目】烃A是一种重要的化工原料。己知A在标准状况下的密度为1.16g·L-1,B可发生银镜反应。它们之间的转化关系如图:请回答:

(1)有机物A中含有的官能团名称是____________。
(2)反应④的原子利用率达100%,该反应的化学方程式是___________。
(3)下列说法正确的是___________。
A 反应⑤合成乙酸乙酯也能实现原子利用率100%
B.反应②、③、⑤的类型各不相同
C 由于乙酸乙酯和水均为无色液体,故用分液漏斗无法分离乙酸乙酯和水的混合物
D.相同条件下乙酸乙酯在氢氧化钠溶液中水解较在稀硫酸中更完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】资料显示:氨气可在纯氧中安静燃烧![]() 某校化学小组学生设计如下装置
某校化学小组学生设计如下装置![]() 图中铁夹等夹持装置已略去
图中铁夹等夹持装置已略去![]() 进行氨气与氧气在不同条件下反应的实验;
进行氨气与氧气在不同条件下反应的实验;

(1)氨气极易溶于水,其水溶液叫做氨水,显______性,能使石蕊试液变______;其原因为____________![]() 用化学方程式和电离方程式表示
用化学方程式和电离方程式表示![]()
(2)图甲是实验室制取纯净、干燥的氨气的装置图,写出大试管内发生反应的化学方程式![]() 采用实验室常用药品制氨气
采用实验室常用药品制氨气![]() :______,A中所加药品为______,所起作用为______.
:______,A中所加药品为______,所起作用为______.
(3)将产生的氨气与过量的氧气通到装置乙中,用酒精喷灯加热后,试管内气体为______色,氨催化氧化的化学方程式是______
(4)将过量的氧气与甲产生的氨气分别从a、b两管进气口通入到装置丙中,并在b管上端点燃氨气,其氧化产物为空气的主要成分之一;
![]() 两气体通入的先后顺序是______;
两气体通入的先后顺序是______;![]() 氨气燃烧的化学方程式是______.
氨气燃烧的化学方程式是______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氧化钠和过氧化钠的叙述中不正确的是
A.Na2O2是淡黄色固体,Na2O是白色固体,阴阳离子个数比均为1:2
B.Na2O2和Na2O均为碱性氧化物,都能与水反应生成NaOH
C.Na2O和Na2O2均能与CO2发生反应,都有Na2CO3生成
D.2gH2充分燃烧后产物被Na2O2完全吸收,Na2O2固体增重2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g)![]() N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
A | B | C | D |
|
|
|
|
升高温度, | 0~3s内,反应速率为: | t1时仅加入催化剂, | 达平衡时,仅改变x,则x为c(O2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有Na+、Ba2+、Cu2+、CO32-、Cl-、Mg2+中的一种或几种离子。
①向此溶液中滴加足量稀盐酸无明显现象。
②取少许①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生。
③取②的上层清液并加入足量的NaOH溶液,有白色沉淀产生。
(1)原溶液中一定含有的离子是________,一定不含有的离子是________,不能确定是否含有的离子是________。
(2)②中反应的离子方程式为___________________。
(3)若另取10mL①的溶液于锥形瓶中,然后向此溶液中逐滴加入NaOH溶液(如图甲所示)。滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如图乙所示。
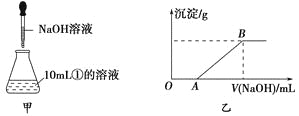
①OA段反应的离子方程式为_____________________。
②AB段反应的离子方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将BaO2放入密闭的真空容器中,反应2BaO2(s)![]() 2BaO(s)+O2(g)达到平衡,保持温度不变,缩小一半容积,体系重新达到平衡,下列说法不正确的是
2BaO(s)+O2(g)达到平衡,保持温度不变,缩小一半容积,体系重新达到平衡,下列说法不正确的是
A. 气体的平均摩尔质量不变 B. BaO量减小
C. BaO2的转化率减小 D. 体积中密度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应2SO2(g)+O2(g) ![]() 2SO3(g),ΔH<0已达平衡,在其他条件不变的情况下,如果分别改变下列条件,对化学反应速率和化学平衡产生影响与图像不相符的是
2SO3(g),ΔH<0已达平衡,在其他条件不变的情况下,如果分别改变下列条件,对化学反应速率和化学平衡产生影响与图像不相符的是
A. 增加氧气浓度 B. 增大压强
B. 增大压强 C. 升高温度
C. 升高温度 D. 加入催化剂
D. 加入催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】叠氮化钠(NaN3)固体易溶于水,微溶于乙醇,不溶于乙醚,是汽车安全气囊中的主要成分,能在发生碰撞的瞬间分解产生大量气体使气囊鼓起。
已知:![]() 。
。
实验室利用如图装置模拟工业级NaN3制备。

实验Ⅰ:制备NaN3
(1)装置C中盛放的药品为____________,装置B的主要作用是__________________。
(2)为了使a容器均匀受热,装置D中进行油浴而不用水浴的主要原因是______________。
(3)氨气与熔化的钠反应生成NaNH2的化学方程式____________________________________。
(4)N2O可由NH4NO3(熔点169.6℃)在240℃分解制得,应选择的气体发生装置是________。

实验Ⅱ:分离提纯
分离提纯反应完全结束后,取出装置D中的混合物进行以下操作,得到NaN3固体。

(5)已知:NaNH2能与水反应生成NaOH和氨气,操作Ⅳ采用__________洗涤,其原因是_____________。
实验Ⅲ:定量测定
实验室用滴定法测定叠氮化钠样品中NaN3的质量分数:
①将2.500g试样配成500.00mL溶液。
②取50.00mL溶液于锥形瓶中,加入50.00mL 0.1010![]() (NH4)2Ce(NO3)6 溶液。
(NH4)2Ce(NO3)6 溶液。
③充分反应后,将溶液稍稀释,向溶液中加入8mL浓硫酸,滴入3滴邻菲啰啉指示液,0.0500![]() (NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+,消耗标准溶液的体积为29.00mL。测定过程中涉及的反应方程式如下:2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑,Ce4++Fe2+=Ce3++Fe3+
(NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+,消耗标准溶液的体积为29.00mL。测定过程中涉及的反应方程式如下:2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑,Ce4++Fe2+=Ce3++Fe3+
(6)配制叠氮化钠溶液时,除烧杯、玻璃棒、量筒外,还需要用到的玻璃仪器有___________。若其它读数正确,滴定到终点后读取滴定管中(NH4)2Fe(SO4)2标准溶液体积时俯视,将导致所测定样品中叠氮化钠质量分数__________(选填“偏大”、“偏小”或“不变”)。
(7)试样中NaN3的质量分数为___________。(保留四位有效数字)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com