
| A. | 改善能源结构,大力发展太阳能、风能等清洁能源 | |
| B. | 推广碳捕集和储存技术,逐步实现二氧化碳零排放 | |
| C. | 推广使用煤液化、气化技术,减少二氧化碳的排放 | |
| D. | 工业废水、生活污水净化处理,减少污染物的排放 |
分析 A.改善能源结构,大力发展太阳能、风能等清洁能源,可减少化石能源的利用,减少了二氧化碳、二氧化硫和粉尘的排放,符合社会可持续发展理念;
B.推广碳捕集和储存技术,逐步实现二氧化碳零排放,减少温室效应;
C.推广使用煤液化技术、气化技术,能使煤燃烧充分,但不能减少二氧化碳的排放;
D.对工业废水、生活污水净化处理,减少污染物的排放,符合社会可持续发展理念.
解答 解:A.改善能源结构,大力发展太阳能、风能等清洁能源,可以减少有害气体和粉尘的产生,能减少雾霾天气发生,符合可持续发展宗旨,故A不选;
B.二氧化碳气体是产生温室效应的主要气体,推广碳捕集和储存技术,逐步实现二氧化碳零排放,减少了二氧化碳的排放,符合社会可持续发展宗旨,故B不选;
C.煤经气化生成一氧化碳和氢气,液化能变为甲醇,燃烧仍生成二氧化碳,故不能减少二氧化碳的排放,不符合可持续发展宗旨,故C选;
D.水污染主要来自工业、农业、生活污染物的排放,工业废水生活污水经过处理后可以节约资源,保护水源,符合社会可持续发展宗旨,故D不选;
故选C.
点评 本题考查环境保护及可持续发展,注意节约资源、开发新能源、走可持续发展之路,人人有责,题目难度不大.


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:推断题
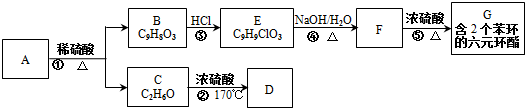
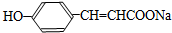 .
.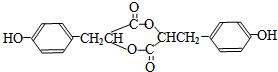 .
.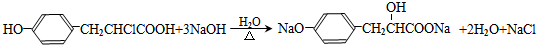 :反应①:
:反应①: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的液化是物理变化 | |
| B. | 纤维素水解产物可以通过一系列化学变化制乙醇 | |
| C. | “歼-20”飞机上使用的碳纤维是一种新型的有机高分子材料 | |
| D. | 漂白粉长期放置会被空气中的氧气氧化而变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | 元素的相关信息 |
| A | 最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐 |
| B | 原子的M电子层上有3个电子 |
| C | 在短周期主族元素中,其原子半径最大 |
| D | 其最外层电子数是电子层数的2倍,且低价氧化物能与其气态氢化物反 应生成D的单质和H2O |
| E | 元素最高正价与最低负价的代数和为6 |
| A. | A的气态氢化物具有还原性,常温下,该氢化物水溶液的pH>7 | |
| B. | C单质在氧气中燃烧后的产物中阴阳离子个数之比为1:2 | |
| C. | 在B和E所形成的化合物中存在离子键 | |
| D. | C与D可形成不同原子或离子个数比的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 羟基的电子式: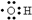 | B. | 淀粉和纤维素的实验式:CH2O | ||
| C. | CH4分子的球棍模型: | D. | 核内有8个中子的碳原子:${\;}_{6}^{8}$C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaAlO2(aq)$\stackrel{CO_{2}}{→}$Al(OH)3$\stackrel{△}{→}$Al2O3(熔融)$\stackrel{电解}{→}$Al | |
| B. | Cu2(OH)2CO3$\stackrel{盐酸}{→}$CuCl2(aq)$\stackrel{电解}{→}$Cu | |
| C. | SiO2$\stackrel{H_{2}O}{→}$H2SiO3$\stackrel{NaOH(aq)}{→}$Na2SiO3(aq) | |
| D. | CuSO4(aq)$\stackrel{NaOH(aq)}{→}$Cu(OH)2悬浊液$→_{△}^{葡萄糖}$Cu2O |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
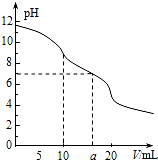 常温下,用 0.1mol•L-1 HCl溶液滴定10.0mL浓度为0.1mol•L-1 Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )
常温下,用 0.1mol•L-1 HCl溶液滴定10.0mL浓度为0.1mol•L-1 Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )| A. | 当V=0时:c(CO32-)>c(HCO3-)>c(OH-)>c(H2CO3) | |
| B. | 当V=5时:3c(CO32-)+3c(HCO3-)+3c(H2CO3)=2c(Na+) | |
| C. | 当V=10时:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| D. | 当V=a时:c(Na+)>c(Cl-)>c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
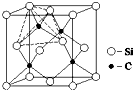 太阳能电池的发展趋向于微型化、薄膜化.最新产品是铜镓(Ga)硒(Se)等化合物薄膜太阳能电池和Si系薄膜太阳能电池.完成下列填空:
太阳能电池的发展趋向于微型化、薄膜化.最新产品是铜镓(Ga)硒(Se)等化合物薄膜太阳能电池和Si系薄膜太阳能电池.完成下列填空:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8gNa2S和Na2O2的混合物中含有的阴离子数目大于0.1NA,小于0.2NA | |
| B. | 常温下0.1mol•L-1的NH4NO3溶液中氮原子数为0.2NA | |
| C. | 标准状况下,2.24L CHCl3的分子数为0.1NA | |
| D. | 19gT35Cl和H37Cl的混合物中所含中子数为10NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com