
| A. | 只有①② | B. | 只有②④ | C. | 只有②③④ | D. | 只有①④ |
分析 醋酸钠溶液中存在醋酸根离子水解平衡:CH3COO-+H2O?CH3COOH+OH-,影响水解平衡移动的因素来回答判断.
解答 解:①加入NaOH固体,会导致氢氧根离子浓度增大,水解平衡向逆向移动,所以醋酸根离子浓度增大,但是钠离子增加的程度大,即比值会减小,故①错误;
②加入KOH固体,钠离子浓度不变,水解平衡向逆向移动,所以醋酸根离子浓度增大,即比值会增大,故②正确;
③加入CH3COONa固体,醋酸根离子以及钠离子浓度均增大,同时会对水解平衡起到抑制作用,所以醋酸根离子浓度增加的程度大,比值增大,故③正确.
④加入冰醋酸,冰醋酸的浓度增大,水解平衡向逆向移动,所以醋酸根离子浓度增大,即比值会增大,故④正确;
故选:C.
点评 本题考查学生盐的水解原理以及影响盐的水解平衡移动等方面的知识,注意知识的归纳整理是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | HF电离:HF(aq)?H+(aq)+F-(aq)△H=+10.4kJ/mol | |
| B. | 水解消耗0.1mol F-时,吸收的热量为6.77kJ | |
| C. | 中和热均为57.3 kJ/mol | |
| D. | 含0.1mol HF、0.1mol NaOH 的两种溶液混合后放出的热量为6.77kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
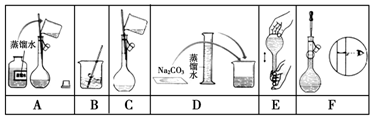
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
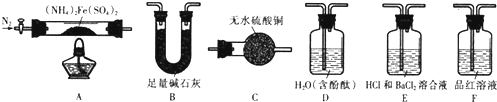
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
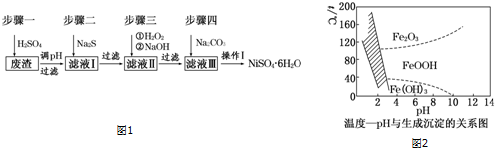
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
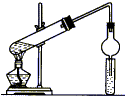 用如图所示装置制取乙酸乙酯,请回答以下问题.
用如图所示装置制取乙酸乙酯,请回答以下问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com