
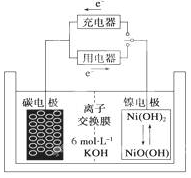
 һ��̼�����ܹ����������������ֲ����Ʊ��Ķ��ε��ԭ����ͼ��ʾ���õ�صĵ����Ϊ6mol•L-1KOH��Һ������˵������ȷ���ǣ�������
һ��̼�����ܹ����������������ֲ����Ʊ��Ķ��ε��ԭ����ͼ��ʾ���õ�صĵ����Ϊ6mol•L-1KOH��Һ������˵������ȷ���ǣ�������| A�� | �ŵ�ʱK+���� | |
| B�� | �ŵ�ʱ��ظ����ĵ缫��ӦΪH2-2e-�T2H+ | |
| C�� | �ŵ�ʱ��������ĵ缫��ӦΪNiO��OH��+H2O+e-�TNi��OH��2+OH- | |
| D�� | �õ�س��ʱ��̼�缫���Դ����������������������Ӧ |
���� A���ŵ�ʱ���������Һ���������������ƶ���
B���ŵ�ʱ������������ʧ���ӷ���������Ӧ��
C���ŵ�ʱ��������NiO��OH���õ��ӷ�����ԭ��Ӧ��
D���õ�س��ʱ��̼�缫���Դ�ĸ���������
��� �⣺A���ŵ�ʱ���õ��Ϊԭ��أ��������Һ���������������ƶ������Լ������������ƶ�����A����
B���ŵ�ʱ������������ʧ���ӷ���������Ӧ���缫��ӦʽΪH2+2OH--2e-�T2H2O����B����
C���ŵ�ʱ��������NiO��OH���õ��ӷ�����ԭ��Ӧ���缫��ӦʽΪNiO��OH��+H2O+e-�TNi��OH��2+OH-����C��ȷ��
D���õ�س��ʱ��̼�缫��������Ҫ�ָ�ԭ״����Ӧ�õõ��ӷ�����ԭ��Ӧ������̼�缫��������Ӧ�����Դ�ĸ�����������D����
��ѡ��C��
���� ���⿼����ԭ��غ͵���ԭ������ȷ�������Ϸ����ĵ缫��Ӧ���������ӵ��ƶ����ɽ���״�ѡ����D��ע���ϵ��ԭ��ȷ����ԭ����ĸ��缫������Ϊ�״��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 1��3-����ϩ��CH2=CHCH=CH2����2-��Ȳ��CH3C CH3������Ҫ���л�ԭ�ϣ�
1��3-����ϩ��CH2=CHCH=CH2����2-��Ȳ��CH3C CH3������Ҫ���л�ԭ�ϣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ˮʯ��������ľ�ϡ����漰��ѧ�仯 | |
| B�� | ���������������Ӿ������������γ� | |
| C�� | ������ˮ��ԭ���͡�84������Һ������ԭ������ͬ | |
| D�� | ����β���к��еĵ�����������Ͳ���ȫȼ����ɵ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �̻�ȼ�ţ�����ͷ����������ijЩ����Ԫ�ص��������� | |
| B�� | ��������������������ЧӦ�������⻯ѧ���������γɶ��뵪�������� | |
| C�� | ���ۺ���ά�ض���ˮ�⣬ˮ�����ղ��ﶼΪ������ | |
| D�� | ����CO2�ϳɾ�̼������ɽ������ϣ�ʵ�֡�̼����ѭ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ˮ�����c�� H+��=1��l0-13 mol/L����Һ�У�K+��Na+��SiO32-��SO42- | |
| B�� | ���ܽ�Al��OH��3����Һ��NH4+��K+��SO42-��HCO3- | |
| C�� | �����Ի�ɫ����Һ��Na+��CO32-��NO3-��SO32- | |
| D�� | 1.0 mol/L��CH3COOH��Һ��K+��Fe3+��NO3-��Cl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 36gþ�������ĵ�������ȫȼ�չ�ת�Ƶĵ�����Ϊ3NA | |
| B�� | �����£�21.0g��ϩ�Ͷ�ϩ�Ļ�������к��е�C-H���ۼ���ĿΪ3NA | |
| C�� | ��״���£�44.8 L NO��22.4 LO2��Ϻ������з�������Ϊ3NA | |
| D�� | 1 molNa2O��Na2O2�����������������������3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH4Cl�ǵ���ʣ�����NH4Cl��Һ�ǵ���� | |
| B�� | Al2O3��������������������ܽ�������Ҳ�����ڰ�ˮ�� | |
| C�� | ��FeCl3��Һ����ӡˢ��·���ԭ����Fe3+���������� | |
| D�� | Fe��OH��3����ı����������ܲ��������ЧӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ������ | Fe��OH��3 | Al��OH��3 | Zn��OH��2 | Mn��OH��2 |
| ��ʼ����ʱ��pH | 2.7 | 4.0 | 6.4 | 7.7 |
| ��ȫ����ʱ��pH | 3.7 | 5.2 | 8.0 | 10.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
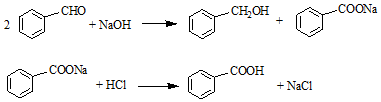
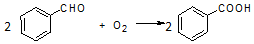
| ���� | ������ | ��״ | ����ܶ� ��g•cm-3�� | �е� ���棩 | �ܽ�� | ||
| ˮ | ���� | ||||||
| ����ȩ | 106 | ��ɫҺ�� | 1.04 | 179 | �� | ���� | |
| ������ | 122 | ��ɫ���� | 1.27 | 249 | 0.21g | 66g | |
| ���״� | 108 | ��ɫҺ�� | 1.04 | 205 | �� | ���� | |
| ���� | 74 | ��ɫҺ�壮 | 0.71 | 35 | ���� | -- | |
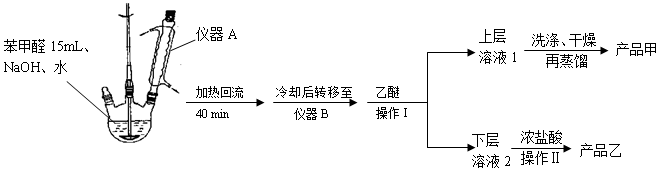
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com