
【题目】D中的反应开始前,需排除装置中的空气,应采取的方法是__________________。
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案科目:高中化学 来源: 题型:
【题目】共价键、金属键、离子键和分子间作用力是微观粒子间的不同相互作用,含有上述两种相互作用的晶体是( )
A. SiO2晶体 B. Ar晶体 C. NaCl晶体 D. NaOH晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下列方法测定某水样中O2的含量。
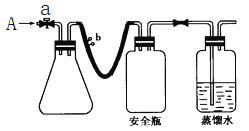
(1)实验原理
①用如图所示装置,使溶解在水中的O2在碱性条件下将Mn2+氧化成MnO(OH)2,反应的离子方程式为_____________________________。
②在酸性条件下,再用I-将生成的MnO(OH)2,还原为Mn2+,反应的离子方程式为_____________________________。然后用Na2S2O3标准溶液滴定生成的I2,反应方程式为I2+2 Na2S2O3=2Na1+Na2S4O6。
(2)实验步骤
①打开止水夹a和b,从A处向装置内鼓入过量N2,此操作的目的是___________________________;
②用注射器抽取某水样20. 00mL从A处注入锥形瓶;
③再分别从A处注入含m mol NaOH溶液及过量的MnSO4溶液;
④完成上述操作后,关闭a、b,将锥形瓶中溶液充分振荡;
⑤打开止水夹a、b,分别从A处注入足量NaI溶液及含n mol H2SO4的硫酸;
⑥重复④的操作;
⑦取下锥形瓶,向其中加入23滴_______作指示剂;
⑧用0.005 mol L -1 Na2S2O3溶液滴定至终点。滴定终点的现象是___________________________。
(3)数据分析
①若滴定过程中消耗的Na2S2O3标准溶液体积为3.90 mL,则此水样中氧(O2)的含量为________ mg L-1。
②若未用Na2S2O3标准溶液润洗滴定管,则测得水样中O2的含量将_________ (填“偏大”“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.氧化镁熔点很高,可作为优质的耐高温材料
B.有色玻璃就是某些胶态金属氧化物分散于玻璃中制成
C.溴化银可用于感光材料,也可用于人工降雨
D.分子筛可用于物质分离,还能作干燥剂和催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关,下列叙述中正确的是
A. 用活性炭为糖浆脱色和用双氧水漂白纸浆,其原理相同
B. 铜制品在潮湿空气中生锈,其主要原因是发生析氢腐蚀
C. 用NaHCO3和Al2(SO4)3溶液可以制作泡沫灭火剂
D. 从海水中可以制取NaCl,电解饱和NaCl溶液可以制取金属Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.向鸡蛋清溶液中加入硫酸铜溶液,鸡蛋清凝聚,蛋白质变性
B.氨基酸种类较多,分子中都含有-COOH和-NH2
C.纤维素、淀粉和蔗糖等天然高分子化合物在一定条件下都能发生水解
D.油脂皂化反应实质就是酯在碱性环境下发生水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子一定能大量共存的是( )
A. 无色溶液中:Na+、Cu2+、NO3-、Cl-
B. 在酸性溶液中:Na+、K+、HCO3-、Cl-
C. 在含Fe2+的溶液中:Na+、Fe3+、I-、Cl-
D. 与铝单质反应产生气体的溶液:Na+、K+、Cl- 、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚CH3OCH3和乙醇CH3CH2OH是同分异构体,其鉴别可采用化学方法及物理方法,下列鉴别方法中不能对二者进行鉴别的是( )
A.元素分析B.质谱C.红外光谱法D.核磁共振氢谱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com