

| A. | a点对应的NH3•H2O溶液的pH=12 | |
| B. | b点混合溶液中:c(C1-)=c(NH4+)+c(NH3•H2O) | |
| C. | c点混合溶液中:c(H+)>[(NH3•H2O)] | |
| D. | d点混合溶液中:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
分析 A.根据电离度=$\frac{已电离的电解质分子数}{溶液中原来电解质的总分子数}$×100%及一水合氨按的浓度计算电离出的氢氧根离子浓度,然后可计算出a点对应的NH3•H2O溶液的pH;
B.b点溶质为等浓度的一水合氨和氯化铵,结合物料守恒分析;
C.c点二者恰好反应生成氯化铵,结合氢离子还来自水的电离分析;
D.d点为等浓度的HCl和氯化铵,铵根离子部分水解,则c(H+)>c(NH4+).
解答 解:A.0.1mol/LNH3•H2O溶液中NH3•H2O的电离度为1%,则该氨水中氢氧根离子浓度为:0.1mol/L×1%=0.001mol/L,该溶液的pH=11,故A错误;
B.b点加入10mL等浓度的盐酸,反应后溶质为等浓度的NH3•H2O和氯化铵,根据物料守恒可得:2c(C1-)=c(NH4+)+c(NH3•H2O),故B错误;
C.c点加入20mL等浓度的盐酸,反应后溶质为氯化铵,铵根离子水解生成NH3•H2O和氢离子,氢离子还来自水的电离,则c(H+)>[(NH3•H2O)],故C正确;
D.d点加入40mL盐酸,反应后溶质为等浓度的HCl和NH3•H2O,由于NH4+发生水解,导致其浓度减小,则c(H+)>c(NH4+),溶液中正确的离子浓度大小为:c(Cl-)>c(H+)>c(NH4+)>c(OH-),故D错误;
故选C.
点评 本题考查酸碱混合的定性判断、离子浓度大小比较等知识,题目难度中等,明确曲线各点溶质组成为解答关键,注意掌握溶液酸碱性与溶液pH的关系,能够根据电荷守恒、物料守恒及盐的水解原理判断离子浓度大小.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 滴定次数 | 样品的质量/g | 稀盐酸的体积/mL | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 0.3000 | 1.02 | 21.03 |
| 2 | 0.3000 | 2.00 | 21.99 |
| 3 | 0.3000 | 0.20 | 20.20 |

查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝酸钠和金刚石 | B. | 晶体硅和水晶 | C. | 冰和干冰 | D. | 氯化钠和氧化镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
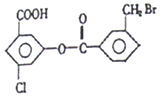 某有机物的结构简式如图:1mol该有机物与足量的氢氧化钠溶液混合并共热,
某有机物的结构简式如图:1mol该有机物与足量的氢氧化钠溶液混合并共热,| A. | 4mol | B. | 5mol | C. | 6mol | D. | 7mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②③④ | C. | ②③⑤ | D. | ①③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com