
(8分)
(1)在水溶液中,YO3n—和S2-发生反应的离子方程式如下:
YO3n—+3S2-+6H+=Y-+3S↓+3H2O,已知Y为1~18号 元素。
元素。
(a)YO3n—中Y的化合价是__________; Y元素原子的最外层电子数是____________;
(b)S2-的半径__________Y-的半径(填“大于”或“小于”)。
(2)在一定条件下A与B反应可生成C和D,其能量变化如下图
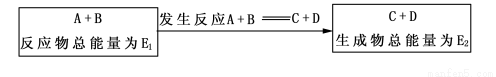
(a)若E1>E2,反应体系的总能量____(填“升高”“降低”),为___(填“吸热”“放热”)反应。
(b)若E1<E2,反应体系的总能量___(填“升高”“降低”),为______(填“吸热”“放热”)反应。
 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源:2014-2015江西省宜春市高二下学期第一次月考化学试卷(解析版) 题型:选择题
化学式为C5H12O2的二元醇有多种同分异构体。其中主链上有3个碳原子和主链上有4个碳原子的二元醇,其同分异构体数目分别是(不包括1个碳原子上连接2个羟基的化合物):
A.1和6 B.1和7 C.2和6 D.2和7
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省台州市高二下学期第一次月考化学试卷(解析版) 题型:选择题
碳碳双键不能自由旋转,所以,R—CH CH—R可能有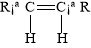 和
和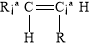 两种空间排列的形式。那么,下列化合物中具有上述两种空间排列形式的是:
两种空间排列的形式。那么,下列化合物中具有上述两种空间排列形式的是:
A.丙烯 B.2 – 戊烯
C.苯乙烯 D.1,3 – 丁二烯
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省达州市高一3月月考化学试卷(解析版) 题型:填空题
(2013·华中师大一附中月考)下表是元素周期表主族元素的一部分,短周期元素X的最高正化合价是+5,Y的单质可在空气中燃烧。
W | X | Y |
Z |
请回答下列问题:
(1)Z的元素符号是 ,写出Z的原子结构示意图: 。
(2)W的最高价氧化物不溶于水,但能溶于烧碱溶液,该反应的离子方程式为 。
(3)探究同主族元素性质的一些共同规律,是学习化学的一项重要内容。在下表中列出对H2ZO3化学性质的推测,举例并写出相应的化学方程式(化学方程式中Z用元素符号表示)
编号 | 性质推测 | 化学方程式 |
示例 | 氧化性 | H2ZO3+4HI=Z↓+2I2+3H2O |
1 | ||
2 |
(4)由C、O和Y三种元素组成的化合物OCY中,所有原子的最外层都满足8电子结构。写出该化合物的电子式: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省达州市高一3月月考化学试卷(解析版) 题型:选择题
国际上不提倡伊朗浓缩铀,因为铀235(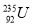 )是制造原子弹的燃料。
)是制造原子弹的燃料。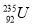 原子核内含有中子数为
原子核内含有中子数为
A.92 B.235 C.143 D.327
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省高一下学期第一次月考化学试卷(解析版) 题型:选择题
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
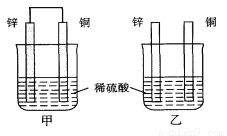
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均减小
D.产生气泡的速度甲比乙快
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省高一下学期第一次月考化学试卷(解析版) 题型:选择题
硒是人体肝脏和肾脏的组成元素之一,现在含有元素硒(Se)的保健品已经进入市场,已知它与氧元素同族,与 K 同周期,关于硒的说法中不正确的是
A.原子序数为 34
B.最高价氧化物的水化物的分子式为:H2SeO4
C.Se的非金属性比 Br 弱
D.气态氢化物的稳定性比硫化氢气体强
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省安庆市高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
为实现实验目的,其他主要仪器,所用试剂合理且需要在某个部位放置温度计的是
选项 | 实验目的 | 玻璃实验仪器 | 实验试剂 | 温度计位置 |
A | 制取乙烯 | 圆底烧瓶、集气瓶、带胶塞导气管、酒精灯 | 浓硫酸、乙醇 | 反应液中 |
B | 提纯乙醇 | 蒸馏烧瓶、冷凝管、锥形瓶、承接管 | 含杂质乙醇 | 支气管口 |
C | 中和热测定 | 烧杯、环形玻璃搅拌器 | 氢氧化钠、醋酸 | 酸、碱及反应液中 |
D | 制镜 | 烧杯、试管、酒精灯 | 银氨溶液、葡萄糖 | 水浴的烧杯水中 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年贵州省八校联盟高三第二次联考理综化学试卷(解析版) 题型:填空题
选考(15)化学与技术
侯氏制碱法的生产流程可表示如下,请回答下列问题:
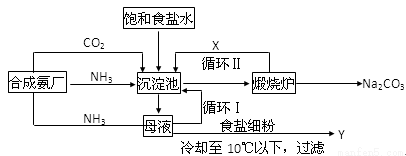
(1)沉淀池中加入(或通入)有关物质的顺序为_____________→___________→___________
(2)写出上述流程中X、Y的化学式:X____________Y___________
(3)写出沉淀池中发生的化学反应方程式__________________________________________
(4)侯氏制碱法的生产流程中可以循环使用的物质主要为____________、______________
(5)从沉淀池中取出沉淀的操作是___________,为了进一步提纯NaHCO3晶体,可采用_______法
(6)若在煅烧炉中燃烧的时间较短,NaHCO3将化解不完全。现若取10.5g NaHCO3固体,加热一定时间后,剩余固体的质量为7.1g,如果把此剩余固体全部加入到200mL 1mol/L的盐酸中,充分反应后溶液中H+的物质的量浓度为___________mol/L(溶液体积变化忽略不计)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com