
 ������Cl-����λ��Ϊ4����֪�������ⳤΪdcm����NA��ʾ�����ӵ�����ֵ�������ܶȱ���ʽΪ$\frac{396}{{d}^{3}•{N}_{A}}$g/cm3��
������Cl-����λ��Ϊ4����֪�������ⳤΪdcm����NA��ʾ�����ӵ�����ֵ�������ܶȱ���ʽΪ$\frac{396}{{d}^{3}•{N}_{A}}$g/cm3�� ���� ��1�����ݺ�������Ų�������дCuԭ�ӵĺ�������Ų�ʽ�����Ӱ��ܲ�ߵͽ���ʧȥ��������дCu2+����Χ�����Ų�ʽ��ͭԪ��λ�����ڱ�ds ����ͬ����������ң��縺�����ݴ��ж�C��O��NԪ�صĵ縺�ԣ�
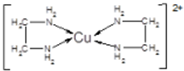
��2���Ҷ�����H2N-CH2-CH2-NH2����Nԭ�ӳ�3���Ҽ�������1�Թ¶Ե��ӣ��ӻ������Ϊ4����ȡsp3�ӻ����Ҷ�����H2N-CH2-CH2-NH2������֮������γ�����������װ�[N��CH3��3]����֮�䲻���γ������
��3�����ݾ���ṹ�ص����Clԭ�ӵ���λ����
��� �⣺��1��Cuԭ�ӵĺ�������Ų�ʽΪ1s22s22p63s23p63d104s1����Cu2+����Χ�����Ų�ʽΪ3d9��
ͬ����������ң��縺������ͬ���ڵڢ�A�塢�ڢ�A�壬�����ڵ�Ԫ�صĵ縺�Դ�����C��O��NԪ�صĵ縺�ԵĴ�СΪ��N��O��C���ʴ�Ϊ��3d9��ds ����N��O��C��
��2���Ҷ�����H2N-CH2-CH2-NH2����Nԭ�ӳ�3���Ҽ�������1�Թ¶Ե��ӣ��ӻ������Ϊ4����ȡsp3�ӻ����Ҷ�����H2N-CH2-CH2-NH2������֮������γ���������װ�[N��CH3��3]����֮�䲻���γ���������Ҷ����ķе�ϸߣ��ʴ�Ϊ��sp3�ӻ����Ҷ�������֮������γ���������װ�����֮�䲻���γ������
��3����CuCl�ľ��������жϣ�ÿ��ͭԭ����4��Cl�����������ȣ���Cu����λ��Ϊ4�����ݻ�ѧʽ��֪Cl����λ��ҲΪ4��������Cuԭ����ĿΪ4��Clԭ����Ŀ=8��$\frac{1}{8}$+6��$\frac{1}{2}$=4��������=4��$\frac{99.5}{{N}_{A}}$g���辧���ⳤΪdcm����g/cm3����d cm��3=4��$\frac{99.5}{{N}_{A}}$����æ�=$\frac{396}{{d}^{3}•{N}_{A}}$g/cm3��
�ʴ�Ϊ��4��$\frac{396}{{d}^{3}•{N}_{A}}$ g/cm3��
���� �����Ƕ����ʽṹ�����ʵĿ��飬�漰��������Ų����縺�ԡ���ѧ�����ӻ���ʽ��ռ乹���жϡ���������ȣ������������þ�̯�����о������㣬�Ƕ�ѧ���ۺ������Ŀ��飬�Ѷ��еȣ�


 ��ѧ��������������Ͼ���ѧ������ϵ�д�
��ѧ��������������Ͼ���ѧ������ϵ�д� �ϴ�̸�������������νӽ̳��Ͼ���ѧ������ϵ�д�
�ϴ�̸�������������νӽ̳��Ͼ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ú�ĸ���ʯ�͵��ѻ����ѽ�����ڻ�ѧ�仯 | |
| B�� | �������ȷ�Ӧ����ұ��Fe��Cr��Mn��W��Na�Ƚ��� | |
| C�� | ����������Ʊ�һ�ȼ����ԭ�������ʿɴ�100% | |
| D�� | SO2��NO2��CO2���ǵ����������Ҫԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
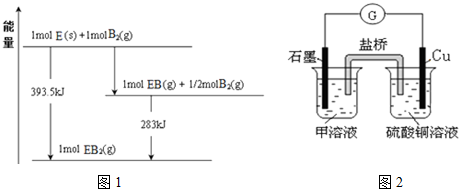
| �� | E | A | B | ||
| C | �� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����м���Ũ�������ַ�������˵��Ũ�����������ˮ�� | |
| B�� | ����ڹ�����������ȼ�տ�������SO3 | |
| C�� | ��SO2ͨ��BaCl2��Һ�����ɰ�ɫ���� | |
| D�� | ���ó���ʯ��ˮ��Һ���� CO2��SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��X��Y�Ļ�����ֻ��2�� | |
| B�� | Y��W������������������� | |
| C�� | ����������Ӧˮ��������ԣ�Y��W | |
| D�� | X��Z�γɵĻ������У���ԭ�Ӿ�����8�����ȶ��ṹ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 150mL 1mol•L-1 NaCl��Һ | B�� | 75mL 2mol•L-1 NH4Cl��Һ | ||
| C�� | 50mL 3mol•L-1KClO3��Һ | D�� | 50mL 1mol•L-1 FeCl3��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2���������� | |
| B�� | KClO3�ڷ�Ӧ�з�����ԭ��Ӧ | |
| C�� | ����5.6LCO2��ת�Ƶĵ�����ĿΪ0.25NA | |
| D�� | 24.5g KClO3�μӷ�Ӧ��ת�Ƶ������ʵ���Ϊ0.2mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��4 | B�� | 2��7 | C�� | 1��2 | D�� | 8��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH4+ | B�� | Mg2+ | C�� | Fe2+ | D�� | Fe3+ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com