
【题目】若A+酸→盐+水,则A不可能属于( )
A. 氧化物 B. 碱 C. 单质 D. 电解质
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
【题目】(1)已知在101 kPa时,32.0 g N2H4(液态)在氧气中完全燃烧生成氮气和H2O,放出热量624 kJ(25 ℃时),N2H4完全燃烧的热化学方程式是__________________。
(2)肼空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼空气燃料电池放电时:
正极的电极反应式是______________________________________;
负极的电极反应式是______________________________________。
(3)如图是一个电解过程示意图。
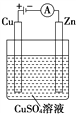
①锌片上发生的电极反应式是_______________________________。
②假设使用肼空气燃料电池作为本过程中的电源,铜片的质量变化为128 g,则肼空气燃料电池理论上消耗标准状况下的空气________L(假设空气中氧气体积分数为20%)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C7H8的芳香烃,在一定条件下与氢气完全加成,加成后产物的一氯代物的同分异构体有( )。
A. 3种 B. 4种 C. 5种 D. 6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1.0 L密闭容器中放入0.10 mol X,在一定温度下发生反应:X(g)![]() Y(g)+Z(g) ΔH<0,容器内气体总压强p随反应时间t的变化关系如图所示。以下分析正确的是
Y(g)+Z(g) ΔH<0,容器内气体总压强p随反应时间t的变化关系如图所示。以下分析正确的是

A.从反应开始到t1时的平均反应速率v(X)=![]() mol/(L·min)
mol/(L·min)
B.该温度下此反应的平衡常数K=0.32
C.欲提高平衡体系中Y的含量,可升高体系温度或减少Z的量
D.其他条件不变,再充入0.1 mol 气体X,平衡正向移动,X的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是元素周期表的一部分,参照元素①~⑧在表中的位置,请用化学用语回答下列问题:
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)④、⑤、⑦的原子半径由大到小的顺序为(元素符号)___________。
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是(填化学式)___________。
(4)由②和④组成的化合物与⑤的同周期相邻主族元素的单质反应的化学方程式为:_____________。
(5)⑦单质与⑤的最高价氧化物的水化物反应的离子方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某恒温恒容密闭容器中,发生如下反应:2A(g)+B(g)![]() 3C(g)+D(s),下列说法能表明该反应已达到平衡状态的是
3C(g)+D(s),下列说法能表明该反应已达到平衡状态的是
A.混合气体的平均相对分子质量不再改变
B.容器内气体的总物质的量不随时间而变化
C.D的浓度不随时间变化而改变
D.单位时间内生成2n mol A的同时,生成n mol的B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不传热的固定容积的密闭容器中发生可逆反应:mA(g)+nB(g)![]() pC(g)+ qQ(g),当m、n、p、q为任意整数时,达到平衡状态的标志是
pC(g)+ qQ(g),当m、n、p、q为任意整数时,达到平衡状态的标志是
①体系的压强不再改变
②体系的温度不再改变
③各组分的浓度不再改变
④各组分的质量分数不再改变
⑤反应速率v(A):v(B):v(C):v(D)=m:n:p:q
⑥单位时间内m mol A断键反应,同时p mol C也断键反应
A.③④⑤⑥ B.②③④⑥
C.①③④⑤ D.①③④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com