

 .
.
 +4NaOH$\stackrel{△}{→}$2CH3COONa+
+4NaOH$\stackrel{△}{→}$2CH3COONa+ +4H2O.
+4H2O. 分析 芳香酯类化合物A、B中一定有苯环,且A、B蒸气对氢气的相对密度是97,则A、B的分子量是194,分子中C、H原子个数相同,且C、H原子总数是氧原子数的5倍,则分子式一定是C10H10O4,芳香酯的同分异构体有 和
和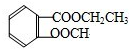 两种,
两种,
A水解生成CD和水杨酸,C能发生银镜反应,则C为HCOOH,D为CH3CH2OH,则A是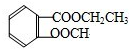 、B是
、B是 ,
,
B水解生成水杨酸、E和F,F经连续氧化可生成C,则F为CH3OH,则E为CH3COOH,
(5)
甲苯和氯气在氯化铁作催化剂条件下发生取代反应生成邻甲基氯苯,邻甲基氯苯被酸性高锰酸钾溶液氧化生成邻氯苯甲酸,则试剂a为酸性高锰酸钾溶液,邻氯苯甲酸在高温高压条件下反应生成M,M酸化得到水杨酸,说明邻氯苯甲酸在碱性条件下发生水解反应生成M ,M酸化得到水杨酸,试剂b为NaOH的水溶液.
,M酸化得到水杨酸,试剂b为NaOH的水溶液.
解答 解:芳香酯类化合物A、B中一定有苯环,且A、B蒸气对氢气的相对密度是97,则A、B的分子量是194,分子中C、H原子个数相同,且C、H原子总数是氧原子数的5倍,则分子式一定是C10H10O4,芳香酯的同分异构体有 和
和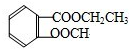 两种,
两种,
A水解生成CD和水杨酸,C能发生银镜反应,则C为HCOOH,D为CH3CH2OH,则A是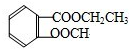 、B是
、B是 ,
,
B水解生成水杨酸、E和F,F经连续氧化可生成C,则F为CH3OH,则E为CH3COOH,
(1)A是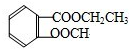 ,A的分子式是C10H10O4,故答案为:C10H10O4;
,A的分子式是C10H10O4,故答案为:C10H10O4;
(2)D为CH3CH2OH,1molD完全燃烧消耗氧气物质的量=(2+$\frac{6}{4}$-$\frac{1}{2}$)mol=3mol,设有机物化学式为CxHyOz,1mol有机物完全燃烧耗氧量=1mol×(x+$\frac{y}{4}$-$\frac{z}{2}$),
完全燃烧时,1mol D与1mol下列有机物耗氧量相同,则(x+$\frac{y}{4}$-$\frac{z}{2}$)=3,
a.C2H4中(x+$\frac{y}{4}$-$\frac{z}{2}$)=2+1-0=3,故正确;
b.C3H8O中(x+$\frac{y}{4}$-$\frac{z}{2}$)=3+2-0.5=4.5,故错误;
c.C2H6O2中(x+$\frac{y}{4}$-$\frac{z}{2}$)=2+2.5-1=3.5,故错误;
d.C3H6O3中(x+$\frac{y}{4}$-$\frac{z}{2}$)=3+1.5-1.5=3,故正确;
故选ad;
(3)水杨酸中的羧基可以和碳酸氢钠发生反应,生成二氧化碳,即: ,故答案为:
,故答案为: ;
;
(4)甲酸中含有醛基,具有还原性,能被银氨溶液氧化,反应方程式为:HCOOH+2Ag(NH3)2OH $\stackrel{水浴加热}{→}$(NH4)2CO3+2Ag↓+2NH3+H2O,属于氧化反应,
故答案为:HCOOH+2Ag(NH3)2OH $\stackrel{水浴加热}{→}$(NH4)2CO3+2Ag↓+2NH3+H2O;
(5)
甲苯和氯气在氯化铁作催化剂条件下发生取代反应生成邻甲基氯苯,邻甲基氯苯被酸性高锰酸钾溶液氧化生成邻氯苯甲酸,则试剂a为酸性高锰酸钾溶液,邻氯苯甲酸在高温高压条件下反应生成M,M酸化得到水杨酸,说明邻氯苯甲酸在碱性条件下发生水解反应生成M ,M酸化得到水杨酸,试剂b为NaOH的水溶液;
,M酸化得到水杨酸,试剂b为NaOH的水溶液;
①通过以上分析知,[条件a]氯化铁作催化剂;(试剂a)为酸性高锰酸钾溶液;(试剂b)为NaOH水溶液,
故答案为:氯化铁作催化剂;酸性高锰酸钾溶液;NaOH水溶液;
②步骤2与步骤3能否交换,不能,因为酚羟基易被氧化,故答案为:不能;酚羟基易被氧化;
(6)同时符合下列要求的化合物,①与A互为同分异构体,说明分子式为C10H10O4;
②可以水解,说明含有酯基;
③苯环上有两个取代基,且苯环上的一氯代物只有1种,说明含有苯环且苯环上只有一种氢原子,
这两个取代基相同且位于对位,
取代基可能是CH3COO-、HCOOCH2-、-COOCH3,所以符合条件的有3种,
故答案为:3;
(7)1mol上述(6)中的一种有机物X在水溶液中,能与4mol NaOH共热发生反应,则X水解生成羧基和酚羟基,则为 ,该反应方程式为
,该反应方程式为 +4NaOH$\stackrel{△}{→}$2CH3COONa+
+4NaOH$\stackrel{△}{→}$2CH3COONa+ +4H2O,
+4H2O,
故答案为: +4NaOH$\stackrel{△}{→}$2CH3COONa+
+4NaOH$\stackrel{△}{→}$2CH3COONa+ +4H2O.
+4H2O.
点评 本题考查有机物推断,为高频考点,涉及物质推断、物质的量的计算、方程式的书写、同分异构体种类判断等知识点,侧重考查学生分析推断能力,正确推断AB结构简式是解本题关键,难点是(2)题计算及(6)题限制型同分异构体种类判断,题目难度中等.


科目:高中化学 来源: 题型:推断题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 物质(杂质) | 所用试剂 | 分离方法 |
| A | 溴苯(Br2) | 苯 | 萃取、分液 |
| B | CO2(HCl) | 饱和NaHCO3溶液 | 洗气 |
| C | C2H4(SO2) | 酸性高锰酸钾 | 洗气 |
| D | CH3CH2OH(H2O) | 生石灰 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用玻璃棒蘸取氯水点在pH试纸上,再与标准比色卡比色测出氯水的pH值 | |
| B. | 检验硫酸钠溶液中的氯离子:取样,滴加1~2滴硝酸银溶液,振荡,溶液变浑浊,则样液中含有Cl- | |
| C. | 可采用冷却结晶的方法从混有KNO3的NaCl溶液中提纯NaCl | |
| D. | 做蒸馏实验一会儿后,发现蒸馏烧瓶中没加沸石,应停止加热,待冷却后补加沸石 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘遇淀粉变蓝,故在厨房里可用米汤检验加碘食盐中的碘 | |
| B. | 煤的气化、液化、干馏以及石油的分馏、裂化、裂解均属化学变化 | |
| C. | 明矾和氯气常用作自来水的净化与消毒,其作用原理相同 | |
| D. | 维生素C有还原性,故苹果汁中加入维生素C可防止变黄 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
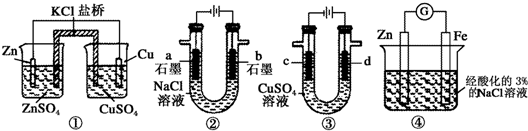
| A. | 装置①中,一段时间后左侧SO42-浓度增大 | |
| B. | 装置②中滴入酚酞,b极附近先变红 | |
| C. | 用装置③精炼铜时,c极为粗铜 | |
| D. | 装置④中在Fe电极附近滴入K3[Fe(CN)6]溶液,可验证Fe电极被保护 |
查看答案和解析>>
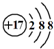
科目:高中化学 来源: 题型:选择题
| A. | 铁原子的质量数均为60 | |
| B. | ${\;}_{26}^{60}$Fe的核内质子数比中子数多8 | |
| C. | 1mol${\;}_{26}^{58}$Fe与足量盐酸反应时均可得到1mol H2 | |
| D. | 等物质的量的${\;}_{26}^{60}$Fe与1mol ${\;}_{26}^{58}$Fe,前者质量比后者多2g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
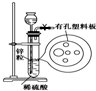 如图为实验室制氢气的简易装置.若在加稀硫酸时发现锌粒与稀硫酸没有接触而稀硫酸不够了,为使该反应顺利进行,可以从长颈漏斗中加入的试剂是( )
如图为实验室制氢气的简易装置.若在加稀硫酸时发现锌粒与稀硫酸没有接触而稀硫酸不够了,为使该反应顺利进行,可以从长颈漏斗中加入的试剂是( )| A. | ①③⑤ | B. | ①②③ | C. | ④⑤⑥ | D. | ①②③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com