
依据元素周期表及元素周期律,下列推断正确的是
A.H3BO3的酸性比H2CO3的强
B.Mg(OH)2的碱性比Be(OH)2的强
C.HCl、HBr、HI的热稳定性依次增强
D.若M+和R2-的核外电子层结构相同,则原子序数:R>M
科目:高中化学 来源: 题型:
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间以下叙述正确的是
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均减小
D.产生气泡的速度甲比乙快
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z为短周期元素,在周期表中的位置如图所示,有关元素W、X、Y、Z的叙述,不正确的是
 A.四种元素的单质中,X的非金属性最强
A.四种元素的单质中,X的非金属性最强
B.四种元素都能与氧元素形成稳定的化合物
C.Y、Z 离子最外层电子数相同
D.Z元素的金属性比Y元素的金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)维生素C的结构简式如下图,它的分子式是________。
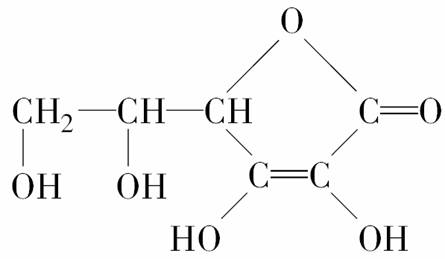
(2)由于它能防治坏血病,又称为抗坏血酸。维生素C溶液中滴入紫色石蕊试液,溶液颜色变红,说明维生素C溶液具有________性;在维生素C溶液中滴入少量蓝色有淀粉的碘水,可观察到的现象是蓝色褪去,说明维生素C具有________性。
(3)用如图所示的实验可以初步比较苹果汁和橙汁中维生素含量的多少。要得出正确的结论,实验过程中不需要控制的条件是________。

A.烧杯的大小必须完全相等
B.烧杯中的淀粉—碘溶液的浓度必须相等
C.胶头滴管滴出的每滴果汁的体积必须相等
D.胶头滴管滴出的滴数必须相等
查看答案和解析>>
科目:高中化学 来源: 题型:
已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性。下列说法正确的是( )
A.X、Y、Z、W的原子半径依次减小
B.W与X形成的化合物中只含离子键
C.W的气态氢化物的沸点一定高于Z的气态氢化物的沸点
D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3
查看答案和解析>>
科目:高中化学 来源: 题型:
四种短周期元素在周期 表中的相对
表中的相对 位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。
位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。
| X | Y | |
| Z | W |
请回答下列问题:
(1)元素Z位于周期表中第______________周期,___________族;
(2)这些元素的氢化物中,水溶液碱性最强的是_______________(写化学式);
(3)XW2的电子式为_______________;
(4)Y的最高价氧化物的化学式为________________;
(5)W和Y形成的一种二元化合物具有色温效应,请相对分子质量在170~190之间,且W的质量分数约为70%。该化合物的化学式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
下列叙述正确的是
A.X、Y元素的金属性 X<Y
B.一定条件下,Z单质与W的常见单质直接生成2W2
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,W单质可以将Z单质从其氢化物中置换出来
查看答案和解析>>
科目:高中化学 来源: 题型:
海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。
(1)在光照条件下,氯气和氢气反应过程如下:
①Cl2 Cl+Cl ②Cl+H2
Cl+Cl ②Cl+H2 HCl+H ③H+Cl2
HCl+H ③H+Cl2 HCl+Cl……
HCl+Cl……
反应②中形成的化合物的电子式为__________________;反应③中被破坏的化学键属于__________________键(填“极性”或“非极性”)。
(2)在短周期主族元素中,氯元素及与相邻元素的原子半径从大到小的顺序是__________________ (用元素符号表示)。与氯元素同周期且金属性最强的元素位于周期表的第__________________周期__________________族。
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是__________________。
a.卤化银的颜色按AgCl、AgBr、AgI的顺序依次加深
b.卤化氢的键长按H—F、H—Cl、H—Br、H—I的顺序依次减小
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
(4)卤素单质的键能大小如下图。由图推断:

①非金属性强的卤素,其单质分子的化学键__________________断裂(填“容易”或“不容易”或“不一定容易”)。
②卤素单质键能大小与键长的关系为:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
题适合使用二期课改新教材的考生解答,B题适合使用一期课改教材的考生解答。
23.(A)
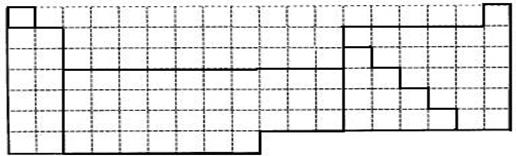
(1)上表中的实线是元素周期表部分边界,请在表中用实线补全元素周期表边界。
(2)元素甲是第三周期ⅥA族元素,请在下边方框中按氦元素(图1)的式样,写出元素甲的原子序数、元素符号、元素名称、相对原子质量和最外电子层排布。

(3)元素乙的3p亚层中只有1个电子,则乙原子半径与甲原子半径比较:_____>_____甲、乙的最高价氧化物水化物的酸性强弱为:_____>_____(用化学式表示)。
(4)元素周期表体现了元素周期律,元素周期律的本质是原子核外电子排布的_________,请写出元素在元素周期表中的位置与元素原 子结构的关系:
子结构的关系:
___________________________________________________
(B)
下表中的实线表示元素周期表的部分边界。①~⑤分别表示元素周期表中对应位置的元素。

(1)请在上表中用实线补全元素周期表边界。
(2)元素⑤的原子核外p电子数比s电子总数多_______个。
元素③氢化物的电子式为_______。
(3)元素④一般在化合物中显_____价,但与_____形成化合物时,所显示的价态则恰好相反。
(4)在元素①的单质、元素②的单质和元素①②形成的合金这三种物质中,熔点最低的是_____。
a.元素①的单质 b.元素②的单质 c.元素①②形成的合金 d.无法判断
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com