科学家一直致力于“人工固氮”的新方法研究.
(1)传统“人工固氮”的反应为N
2(g)+3H
2(g)?2NH
3(g).一定温度下,将1molN
2和3molH
2通入到体积为0.5L的密闭容器中,达到平衡状态时H
2的转化率为50%,该温度下该反应的平衡常数K=
(用分数表示).
(2)最新“人工固氮”的研究报道:常温常压、光照条件下,N
2在催化剂表面与水发生反应:2N
2(g)+6H
2O(l)═4NH
3 (g)+3O
2(g)△H=Q kJ?mol
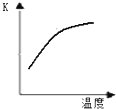
-1①已知该反应的平衡常数K与温度的关系如右图,则此反应的Q
>
>
0 (填“>”“<”或“=”).
②将反应生成的混合气体通入水中即可得氨水.用水稀释0.1mol?L
-1氨水,溶液中随着水量的增加而增大的是
D
D
(填字母标号).
A.
B.
C.c(H
+)?c(OH
-) D.
(3)氨催化氧化法制硝酸的主要反应为:4NH
3(g)+5O
2(g)═4NO(g)+6H
2O(g)△H<0;在容积为1升的密闭容器中发生该反应,容器内部分物质的含量如下表:
| 时间/物质的量 |
n(NH3) (mol) |
n(O2 ) (mol) |
n(NO) (mol) |
| 起始 |
1.600 |
3.200 |
0.000 |
| 第2min |
a |
2.700 |
0.4000 |
| 第4min |
0.600 |
1.950 |
1.000 |
| 第6min |
0.600 |
1.950 |
1.000 |
①反应在第2min到第4min时,NH
3的平均反应速率为
0.3
0.3
mol/(L?min).
②对于上述反应的下列判断,正确的是
D
D
(填序号).
A.若升高反应体系的温度,平衡时体系中NH
3%将减小
B.若增大反应体系的压强,平衡时体系中NO%将增大
C.若升高反应体系的温度,平衡时体系中H
2O%将增加
D.不论该反应是否在催化剂存在的条件下进行,平衡时体系中O
2%保持不变.

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案 (2010?聊城二模)I.科学家一直致力于“人工固氮”的新方法研究.
(2010?聊城二模)I.科学家一直致力于“人工固氮”的新方法研究. 4NH3 (g)+3O2(g)△H=a kJ?mol-1
4NH3 (g)+3O2(g)△H=a kJ?mol-1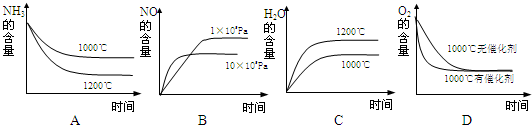
 科学家一直致力于“人工固氮”的新方法研究.
科学家一直致力于“人工固氮”的新方法研究.