
| HA | H2B | HC | ||
| Ka | Ka1 | Ka2 | Ka3 | Ka4 |
| ��ֵ | ||||
���� ��1��������Һ��ǿ���������ԭ���Լ�����Խǿ����ƽ�ⳣ��Խ�����ش�
��2��������0.1mol/LCH3COOH��Һ��ˮϡ�ͣ�c��H+����С��c��OH-������Kw���䣬���볣�����䣬�ݴ˷�����
��3��ϡ����ͬ�ı�����HX��pH�仯�̶ȴ�������HXǿ������ƽ�ⳣ����
��� �⣺��1��������Һ��ǿ���������ԭ���Լ���ӦHA+HB-��������=A-+H2B��H2B��������+C-=HB-+HC��HA��������+C-=A-+HC������ȷ������ǿ���ǣ�HA��H2B��HC��HB-������Խǿ������ĵ���ƽ�ⳣ��Խ��
��
| HA | H2B | HC | ||
| Ka | K a1 | K a2 | K a3 | K a4 |
| ��ֵ | 1.8��10-5 | 4.3��10-7 | 5.6��10-11 | 4.9��10-10 |
| HA | H2B | HC | ||
| Ka | K a1 | K a2 | K a3 | K a4 |
| ��ֵ | 1.8��10-5 | 4.3��10-7 | 5.6��10-11 | 4.9��10-10 |
���� ���⿼�����ƽ�ⳣ�������ԵıȽϡ�pH�����ϡ�͵�֪ʶ��ע��ˮ�������Խ��Խˮ���ϡ����ǿ�ı仯������������ۺ��Խϴ���Ŀ�Ѷ��еȣ���Ҫѧ���߱���ʵ�Ļ������Լ��Ϻõķ���Ӧ��������


 ��ʦ����ɳ���ʱͬ��ѧ����ϵ�д�
��ʦ����ɳ���ʱͬ��ѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ͻ�������п�����ʵ���֮��Ϊ0.02mol | |
| B�� | �Ͻ���ͭ��������ȷ�� | |
| C�� | �Ͻ�������ͭ�����ʵ���֮��Ϊ0.01mol | |
| D�� | 1.30g������п����֮�ͣ�1.12g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
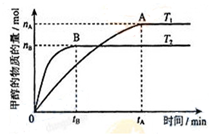 �״�����Ҫ�Ļ���ԭ�ϣ����úϳ�������Ҫ�ɷ�ΪCO��CO2��H2���ڴ�����������
�״�����Ҫ�Ļ���ԭ�ϣ����úϳ�������Ҫ�ɷ�ΪCO��CO2��H2���ڴ����������� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
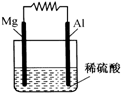 ��ͼ��ʾ��
��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
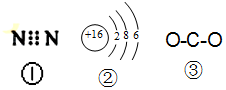
| A�� | ͼ�еĢ���N2�ĵ���ʽ | |
| B�� | ͼ�еĢ���S2-�Ľṹʾ��ͼ | |
| C�� | ������Ϊ53��������Ϊ78�ĵ�ԭ�ӣ�13153I | |
| D�� | ͼ ��ΪCO2�Ľṹʽ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
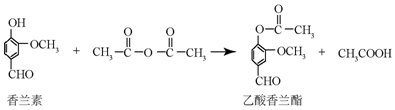
| A�� | �����������ķ���ʽΪC18H8O4 | |
| B�� | FeCl3��Һ���������������������������� | |
| C�� | 1mol������������������5molH2�����ӳɷ�Ӧ | |
| D�� | ��������֬������NaOH��Һ��ˮ��õ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ˮ���廯����Һ��Ӧ��Cl2+2Br-�T2Cl-+Br2 | |
| B�� | ̼��ƺ�ϡ���ᷴӦ��CaCO3+2H+�TCa2++H2O+CO2�� | |
| C�� | ���������������Һ��Ӧ��H++OH-�TH2O | |
| D�� | ��������������Һ��Ӧ��Al+2H2O+OH-�TAlO2-+2H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
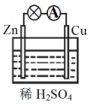
| A�� | ZnΪ������CuΪ���� | B�� | ������пƬͨ����������ͭƬ | ||
| C�� | ������ӦʽΪCu-2e-Cu2+ | D�� | ԭ��صķ�Ӧ������������ԭ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2 | B�� | H2 | C�� | H2O | D�� | O2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com