
| A、1×10-13mol/L |
| B、1×10-3mol/L |
| C、1×10-7mol/L |
| D、1×10-11mol/L |
 作业辅导系列答案
作业辅导系列答案科目:高中化学 来源: 题型:
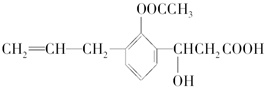
| A、①②③④⑥ | B、②④⑥ |
| C、②④⑤⑥ | D、①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO为氧化产物,H2为还原产物 |
| B、CaCN2中含有非极性键 |
| C、HCN既是氧化剂又是还原剂 |
| D、每消耗10g CaCO3生成2.24L CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向0.01 mol?L-1醋酸溶液中加水,溶液中水电离产生的c(H+) 将减小 | ||
| B、将水加热,KW增大,pH不变,仍呈中性 | ||
| C、向水中加入少量碳酸氢钠固体,溶液的c(H+) 增大,KW不变 | ||
D、c(H+)=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
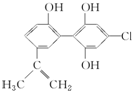 禁止运动员使用兴奋剂是保证比赛公平、公正的重要举措之一.其中一种兴奋剂X的结构如图所示.下列说法不正确的是( )
禁止运动员使用兴奋剂是保证比赛公平、公正的重要举措之一.其中一种兴奋剂X的结构如图所示.下列说法不正确的是( )| A、1 mol X与足量NaOH溶液反应,最多消耗3 mol NaOH |
| B、1 mol X与足量浓溴水反应,最多消耗4 mol Br2 |
| C、X遇FeCl3溶液显色,可看作酚类物质 |
| D、兴奋剂X所有碳原子有可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④⑧ | B、②④⑤⑧ |
| C、③④⑥⑦ | D、④⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com