
【题目】取等物质的量浓度的NaOH溶液两份A和B,每份100 mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol·L-1的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:

(1)原NaOH溶液的物质的量浓度为________。
(2)曲线A表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为________ L。
(3)曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是________________,其物质的量之比为________。
(4)曲线B表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是________________,其物质的量之比为________。
【答案】 0.075 mol·L-1 0.0336 NaOH、Na2CO3 3∶1 Na2CO3、NaHCO3 1∶1
【解析】(1)加入75mL盐酸时二氧化碳的体积达最大,此时溶液为氯化钠溶液。根据氯离子、钠离子守恒,所以n(NaOH)=n(NaCl)=n(HCl)=0.075ml×0.1mol/L=0.0075mol,所以c(NaOH)=![]() =0.075mol/L;(2)CO2与NaOH反应为①CO2+NaOH=NaHCO3,②CO2+2NaOH=Na2CO3+H2O,当n(CO2):n(NaOH)≥1,反应按①进行,n(CO2):n(NaOH)=1时,CO2、NaOH恰好反应生成NaHCO3;n(CO2):n(NaOH)>1时,生成生成NaHCO3,CO2有剩余;当
=0.075mol/L;(2)CO2与NaOH反应为①CO2+NaOH=NaHCO3,②CO2+2NaOH=Na2CO3+H2O,当n(CO2):n(NaOH)≥1,反应按①进行,n(CO2):n(NaOH)=1时,CO2、NaOH恰好反应生成NaHCO3;n(CO2):n(NaOH)>1时,生成生成NaHCO3,CO2有剩余;当![]() <n(CO2):n(NaOH)<1,反应按①②进行,CO2、NaOH反应,无剩余,生成物为NaHCO3、Na2CO3;当n(CO2):n(NaOH)≤
<n(CO2):n(NaOH)<1,反应按①②进行,CO2、NaOH反应,无剩余,生成物为NaHCO3、Na2CO3;当n(CO2):n(NaOH)≤![]() ,反应按②进行,等于
,反应按②进行,等于![]() ,时,CO2、NaOH恰好反应生成Na2CO3;小于
,时,CO2、NaOH恰好反应生成Na2CO3;小于![]() 时,生成Na2CO3,NaOH有剩余;由曲线A可知从60ml到75ml为碳酸氢钠与盐酸反应,反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,所以n(NaHCO3)=n(HCl)=(0.075-0.06)L×0.1mol/L=1.5×10-3mol,根据C原子守恒,所以n(CO2)=n(NaHCO3)=1.5×10-3mol,由(1)可知,n(NaOH)=0.0075mol,所以n(CO2):n(NaOH)=1.5×10-3mol:0.0075mol=1:5,小于1:2,所以反应按②进行,NaOH有剩余,溶液中溶质为Na2CO3和NaOH。
时,生成Na2CO3,NaOH有剩余;由曲线A可知从60ml到75ml为碳酸氢钠与盐酸反应,反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,所以n(NaHCO3)=n(HCl)=(0.075-0.06)L×0.1mol/L=1.5×10-3mol,根据C原子守恒,所以n(CO2)=n(NaHCO3)=1.5×10-3mol,由(1)可知,n(NaOH)=0.0075mol,所以n(CO2):n(NaOH)=1.5×10-3mol:0.0075mol=1:5,小于1:2,所以反应按②进行,NaOH有剩余,溶液中溶质为Na2CO3和NaOH。
(2)根据C原子守恒,所以n(Na2CO3)=n(CO2)=1.5×10-3mol,V(CO2)=1.5×10-3mol×22.4L/mol=0.0336L;
(3)再根据钠离子守恒,得溶液中氢氧化钠的物质的量为0.0075mol-1.5×10-3mol×2=0.0045mol,所以溶液中NaOH与Na2CO3的物质的量之比为0.0045mol:1.5×10-3mol=3:1;
(4)由曲线B可知从25ml到75ml为碳酸氢钠与盐酸反应生成二氧化碳,反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,所以n(NaHCO3)=n(HCl)=(0.075ml-0.025ml)×0.1mol/L=0.005mol,由(1)可知,n(NaOH)=0.0075mol,所以n(CO2):n(NaOH)=0.005mol:0.0075mol=2:3,大于1:2,小于1,所以反应按①②进行,CO2、NaOH反应,无剩余,生成物为NaHCO3、Na2CO3;根据钠原子守恒,所以![]() n(Na2CO3)+ n(NaHCO3)=0.0075mol,而n(NaHCO
n(Na2CO3)+ n(NaHCO3)=0.0075mol,而n(NaHCO


科目:高中化学 来源: 题型:
【题目】用标准的盐酸滴定未知浓度的NaOH溶液,下列操作不会引起实验误差的是( )
A. 用蒸馏水洗净酸式滴定管后,装入标准盐酸进行滴定
B. 用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,后装入NaOH溶液进行滴定
C. 用碱式滴定管取10.00 mL NaOH溶液放入用蒸馏水洗净的锥形瓶中,再加入适量蒸馏水进行滴定
D. 用酚酞作指示剂滴至红色刚变无色时即停止加盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成正丁醛的实验装置如图所示。
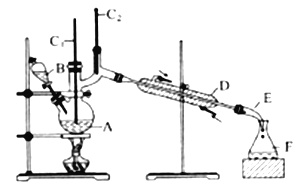
发生的反应如下:CH3CH2CH2CH2OH![]() CH3CH2CH2CHO
CH3CH2CH2CHO
(正丁醇) (正丁醛)
反应物和产物的相关数据列表如下:
沸点/℃ | 密度(g·cm-3) | 水中溶解性 | |
正丁醇 | 11.72 | 0.8109 | 微溶 |
正丁醛 | 75.7 | 0.8017 | 微溶 |
实验步骤如下:
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中在A中加入4.0g 正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90~95℃在F中收集90℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g。回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,并说明理由________。
(2)加入沸石的作用是________。若加热后发现未加沸石,应采取的正确方法是________。
(3)上述装置图中,E仪器的名称是________,D仪器的名称是________。
(4)分液漏斗使用前必须进行的操作是________(填正确答案标号)。
a.润湿 b.干燥 c.检漏 d.标定
(5)将正丁醛粗产品置于分液漏斗中分水时,水在________层(填“上”或“下”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】断开1 mol AB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A—B键的键能。下表列出了一些化学键的键能E:
化学键 | H—H | Cl—Cl | O===O | C—Cl | C—H | O—H | H—Cl |
E/kJ·mol-1 | 436 | 247 | x | 330 | 413 | 463 | 431 |
请回答下列问题:
(1)如图表示某反应的能量变化关系,则此反应为 (填“吸热”或“放热”)反应,其中ΔH=
(用含有a、b的关系式表示)。
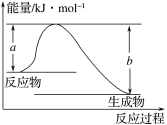
(2)若图示中表示反应H2(g)+![]() O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1,则b= kJ·mol-1,x= 。
O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1,则b= kJ·mol-1,x= 。
(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃利用空气中的氧气跟氯化氢反应制氯气。反应的化学方程式为 。若忽略温度和压强对反应热的影响,根据上题中的有关数据,计算当反应中有1 mol电子转移时,反应的热量变化为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12分)以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:
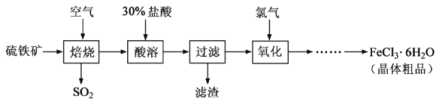
回答下列问题:
(1)在一定条件下,SO2转化为SO3的反应为2SO2(g)+O2(g)![]() 2SO3(g),该反应的平衡常数表达式为K= ;过量的SO2与NaOH溶液反应的化学方程式为
2SO3(g),该反应的平衡常数表达式为K= ;过量的SO2与NaOH溶液反应的化学方程式为
(2)酸溶及后续过程中均需保持盐酸过量,其目的是 、 。
(3)通氯气氧化时,发生的主要反应的离子方程式为
该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为 (写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:
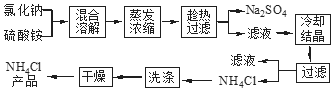

氯化铵和硫酸钠的溶解度随温度变化如上图所示。回答下列问题:
(1)写出制备 NH4Cl的化学方程式:_____________ 。
(2)实验室进行蒸发浓缩用到的主要仪器有___________、烧杯、玻璃棒、酒精灯等。
(3)实验过程中趁热过滤的目的是____________________。
(4)趁热过滤后,滤液冷却结晶。一般情况下,下列哪些因素有利于得到较大的晶体____。
A.缓慢冷却溶液 B.溶液浓度较高 C.溶质溶解度较小 D.缓慢蒸发溶剂
(5)若NH4Cl产品中含有硫酸钠杂质,进一步提纯产品的方法是____________。某研究性学习小组为测定该NH4Cl产品中氮的含量,设计了如图装置,并进行了讨论。
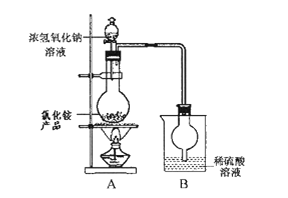
甲同学:根据此实验测得的数据,计算的NH4Cl产品的含氮量可能偏高,因为实验装置中存在一个明显缺陷是:____________________________。
乙同学:实验过程中,往烧瓶中加入的浓氢氧化钠溶液一定要足量并充分加热,原因是___________________________________________。
用改进后的实验装置重新进行实验,称取13.5gNH4Cl产品,测得实验后B装置增重3.4g。则该化肥含氮量为___________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. CH3-CH=CH2分子中所有原子一定处于同一平面
B. 除去乙烷中的乙烯是将混和气体通入酸性KMnO4溶液中
C. 若烃中碳、氢元素的质量分数相同,它们可能是同系物
D. 某烷烃的命名为3,4,4-三甲基己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,纵轴表示导电能力,横轴表示所加溶液的量,下列说法正确的是( )
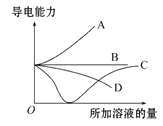
A. 曲线A表示NaOH溶液中滴加稀盐酸
B. 曲线B表示CH3COOH溶液中滴加KOH溶液
C. 曲线C表示Ba(OH)2溶液中滴加稀硫酸
D. 曲线D表示Cu(OH)2悬浊液中滴加HNO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com